
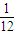 变为12C原子质量的
变为12C原子质量的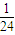 .所以将12C的原子量定为24时,物质的式量加倍.而将阿伏加德罗常数由12g12C所含碳原子数变为24g12C所含原子个数.所以摩尔质量、气体摩尔体积都应加倍,而物质的量及物质的量浓度均随之发生变化.
.所以将12C的原子量定为24时,物质的式量加倍.而将阿伏加德罗常数由12g12C所含碳原子数变为24g12C所含原子个数.所以摩尔质量、气体摩尔体积都应加倍,而物质的量及物质的量浓度均随之发生变化.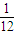 变为
变为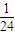 ,所以16O的原子量由16变为32,故A正确;
,所以16O的原子量由16变为32,故A正确;

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源:不详 题型:单选题
| A.此时16O的相对原子质量为32 |
| B.标况下44gCO2的体积为22.4L |
| C.NA个氧分子与NA个氢分子有相同数目的分子 |
| D.44gCO2和28gCO含有相同数目的分子 |
| E.标况下,1molO2为44.8L |
| F.40gNaOH溶于水配成1L溶液,其物质的量浓度为1mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
假定把12C的相对原子质量定为24,把24g12C含有的原子个数定为阿伏加德罗常数,而物质的量的概念不变。则下列推断不正确的是…………( )
A、此时16O的相对原子质量为32
B、标况下44gCO2的体积为22.4L
C、NA个氧分子与NA个氢分子有相同数目的分子
D、44gCO2和28gCO含有相同数目的分子
E、标况下,1molO2为44.8L
F、40gNaOH溶于水配成1L溶液,其物质的量浓度为1mol·L-1
查看答案和解析>>
科目:高中化学 来源:0101 期中题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com