
某同学为研究硝酸与镁的反应,进行图示实验,实验现象及相关数据如下:(a)A中为一定浓度的硝酸与Mg片发生反应,生成的气体通过B后,在B中只生成一种盐,剩余气体遇空气不变色,其体积为原体积的一半。(b)从C进入D中的气体有两种,且体积比为1∶1。(c)将D加热一段时间后,E中干燥的红色石蕊试纸逐渐变蓝。(设实验前,装置中的空气已排尽;气体的体积均在同温同压下测定)

已知2NO2+2NaOH===NaNO3+NaNO2+H2O,NO2+NO+2NaOH===2NaNO2+H2O,且水蒸气的体积忽略不计,实验中的液体药品均过量。请回答:
(1)硝酸与Mg片反应生成的气体成分是________________________________ ____________________________________________(用化学式表示)。
(2)硝酸在装置A的反应中所表现的性质有_________________________ ____________________________________________________。
(3)写出D中发生反应的化学方程式:______________________________ ____________________________________________________________。
(4)若向反应后的A中加入足量的NaOH固体,使产生的气体全部逸出,其体积为硝酸与Mg片反应生成的气体体积的 (同温同压),写出符合上述实验事实的硝酸与Mg片反应的离子方程式_______________________________ ___________________________________________________________。
(同温同压),写出符合上述实验事实的硝酸与Mg片反应的离子方程式_______________________________ ___________________________________________________________。
解析 NO2与NaOH溶液反应的化学方程式为2NO2+2NaOH===NaNO3+NaNO2+H2O,NO与NaOH溶液不反应,但有NO2+NO+2NaOH===2NaNO2+H2O,结合(a)说明产物中有NO和NO2两种气体且两者的体积之比为1∶1。结合(a)(b)知Mg和HNO3反应的产物中有4种气体,且物质的量相等。结合(c)可知进入E中的气体是NH3和水蒸气,反推知从C进入D中的气体由N2和H2组成。通过(4)说明HNO3的还原产物中还存在NH ,其物质的量和每一种气体的物质的量相等,最后可根据得失电子守恒把离子方程式配平。
,其物质的量和每一种气体的物质的量相等,最后可根据得失电子守恒把离子方程式配平。
答案 (1)NO、NO2、N2、H2 (2)酸性、氧化性
(3)Fe2O3+3H2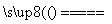 2Fe+3H2O
2Fe+3H2O
N2+3H2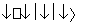 2NH3
2NH3
(4)12Mg+30H++5NO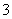 ===12Mg2++NH
===12Mg2++NH +NO2↑+NO↑+N2↑+H2↑+12H2O
+NO2↑+NO↑+N2↑+H2↑+12H2O


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
室温下,若溶液中由水电离产生的c(OH-)=1×10-14mol/L,满足此条件的溶液中一定可以大量共存的离子组是 ( )
A.Al3+、Na+、NO3-、Cl- B.K+、Na+、Cl-、NO3-
C.K+、Na+、Cl-、AlO2- D.K+、NH4+、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
洗衣粉的主要成分之一是烷基苯磺酸钠,常用的是十二烷基苯磺酸钠,其合成路线如下:

请回答下列问题:
(1) 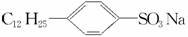 分子中的亲水基是__________,亲油基是__________。
分子中的亲水基是__________,亲油基是__________。
(2)由十二烷基苯制取十二烷基苯磺酸的化学方程式为___________,反应类型为____________________________________________________________。
(3)用油脂可以制肥皂,从硬脂酸甘油酯生成硬脂酸钠和甘油的化学方程式为__________________________________________________,反应类型为________________________________________________________________。
(4)在洗涤剂中添加酶制剂能促进污垢中的蛋白质(如奶渍、肉汤)等水解为可溶性的物质而被除去。使用加酶洗衣粉的水溶液中浸泡10~30 min,水温在40~50 ℃最佳。加酶洗衣粉不宜在高温、潮湿环境中贮存,也不宜久存。为什么? __________________________________________________________。
(5)过去使用的合成洗涤剂中常加入三聚磷酸钠(Na5P3O10)作助剂,它可使硬度大的洗涤水软化,对微细的无机粒子或油脂具有分散、乳化、胶溶作用,防止污渍再次沉积到衣物上;它还能维持水溶液的弱碱性,提高洗涤剂的去污能力和洗涤效果。但是,20世纪90年代以来,世界各国先后提出必须生产和使用无磷洗涤剂。请解释原因______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关氨的说法不正确的是 ( )。
A.NH3是4核10电子分子,具有还原性
B.NH3极易溶于水,可做喷泉实验,氨气易液化,液氨可用作制冷剂
C.氨气是非电解质,NH3·H2O是电解质
D.蘸有浓盐酸的玻璃棒遇氨气产生的白烟为二者挥发产生的酸雾
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将等质量的铜片、银片、铁片、铝片分别置于四个小烧杯中,然后分别加入足量的浓硝酸,放出NO2气体最多的是 ( )。
A.铜片 B.银片
C.铁片 D.铝片
查看答案和解析>>
科目:高中化学 来源: 题型:
长征2号火箭承担运载“神六”的使命,氕化锂、氘化锂、氚化锂可以作为启动长征2号(CZ2F)火箭的优良炸药。下列说法正确的是 ( )。
A.LiH、LiD、LiT的摩尔质量之比为1∶2∶3
B.它们都是强氧化剂
C.H、D、T之间互称为同素异形体
D.它们都是强还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y元素原子最外层电子数与核外电子总数之比为3∶4,M元素原子的最外层电子数与次外层电子数之比为3∶4,且M原子的质子数是Y原子的2倍;N-、Z+、X+的半径逐渐减小;化合物XN在常温下为气体。据此回答下列问题:
(1)写出Z与N形成的化合物的电子式____________。
(2)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式_____________________________________ _________________________________________(分解反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
1 mol某烃在氧气中充分燃烧,需要消耗氧气179.2 L(标准状况下)。它在光照的条件下与氯气反应能生成3种不同的一氯取代物。该烃的结构简式是( )

查看答案和解析>>
科目:高中化学 来源: 题型:
保护环境是公民的责任和义务。下列说法正确的是 ( )。
A.大量使用含磷洗涤剂会带来白色污染
B.减少使用氟氯代烷的目的是为了减少酸雨
C.大量开采地下水,以满足社会对水的需求
D.北京城区限制冬季燃煤供暖,是因为燃烧煤会有二氧化硫产生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com