
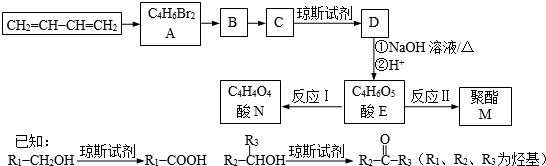
| △ |
| 催化剂 |
 +nH2O;故答案为:HOOCCHBrCH2COOH+3NaOH
+nH2O;故答案为:HOOCCHBrCH2COOH+3NaOH| △ |
| 催化剂 |
 +nH2O;
+nH2O;


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
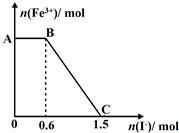 已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )| A、图中AB段的氧化剂为K2Cr2O7 |
| B、图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C、若将上述过程中的KI溶液换为K3[Fe(CN)6]溶液,则有蓝色沉淀生成 |
| D、开始加入的K2Cr2O7为0.25 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下pH=1的一元酸和pH=13的一元碱等体积混合所得溶液一定呈中性 |
| B、常温下,pH=7的氨水与氯化铵的混合溶液中,Cl-与NH4+的浓度关系c(Cl-)>c(NH4+) |
| C、10mL 0.10mol?L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是C(Na+)>C(CH3COO-)>C(OH-)>C(H+) |
| D、中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | NaHCO3固体 | Na2CO3固体 | / | 加热 |
| B | Al2O3 | Fe2O3 | 盐酸 | 过滤 |
| C | KBr溶液 | Br2 | KOH溶液 | 分液 |
| D | Cl2 | HCl | 饱和食盐水 | 洗气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某气体可以使燃着的木条熄灭,说明该气体是CO2 |
| B、向某溶液中滴加AgNO3溶液,有生成白色,说明原溶液中含有Cl- |
| C、向某溶液中滴加用HNO3酸化的AgNO3溶液有白色沉淀产生,说明原溶液中含有Cl- |
| D、向某溶液中滴加BaCl2溶液,有白色沉淀产生,说明原溶液中可能存在CO32-或者SO42 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl的相对分子质量与6.02×1023个HCl分子的质量(以g为单位)在数值上相等 |
| B、6.02×1023个氮分子和6.02×1023个氢分子的质量比等于14:1 |
| C、32 g氧气所含的原子数目为2×6.02×1023 |
| D、常温常压下,0.5×6.02×1023个一氧化碳分子所占体积是11.2 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、我国自主研发的“龙芯1号”CPU芯片与光导纤维是同种材料 |
| B、需要通过化学反应才能从海水中获得食盐和淡水 |
| C、水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| D、粗硅制备单晶硅涉及氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④⑦ | B、②⑤⑦ |
| C、③⑥⑦ | D、全有关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com