
����һƿ1 000 mL����25% NaClO���ܶ���1.19 g��cm-3�ġ�84����Һ����ʹ��ʱ��Ҫϡ��100��������ȣ����ܷⱣ�档���з�������ȷ����
A. �á�84����Һ����NaClO���ʵ���Ũ��Ϊ4.0 mol��L-l
B. �á�84����Һ��ϡ��100����Na+�����ʵ���Ũ��Ϊ0. 04 mol��L-l
C. �����е�CO2�롰84����Һ��������Ӧ�Ļ�ѧ����ʽ��NaClO+CO2+H2O= NaHCO3+ HClO
D. ������ƿ��������Ũ�ȵġ�84����Һ��480 mL����Ҫ������NaClO��������Ϊ143.0 g
 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д� Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�ϲ��и�һ��ѧ�ڷְ�Ի�ѧ�Ծ��������棩 ���ͣ������
��һ����Һ�����ܺ��д�����Mg2����Fe3����Al3����Cu2����Na����H����SO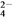 ��CO
��CO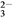 �е�һ�ֻ��֣�ȡ����Һ������ʵ�飺
�е�һ�ֻ��֣�ȡ����Һ������ʵ�飺
��ȡ������Һ�����������ữ��BaCl2��Һ���а�ɫ�������ɣ�
��ȡ������Һ����������Ʒ�ĩ����Һ���а�ɫ�����������ݳ���ɫ��ζ�����壬����Na2O2�����ʵ������������������ʵ�����ͼ��ʾ�����ƶϣ�
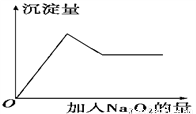
(1)��Һ��һ�����е�������______________��
(2)��Һ�п϶������е�������________________��
(3)���ܺ��е�������____________,��Ҫȷ�������ӵĴ�����Ҫ�õ���ʵ�鷽����____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡĵ�����и߶���ѧ�ڿ�ѧ��⻯ѧ�Ծ��������棩 ���ͣ������
��ѧ��һֱ�����ڡ��˹��̵����ķ����о���
��1��Ŀǰ�ϳɰ��ļ���ԭ��Ϊ��N2(g)+3H2(g) 2NH3(g) ��H �÷�Ӧ�������仯��ͼ��ʾ��
2NH3(g) ��H �÷�Ӧ�������仯��ͼ��ʾ��
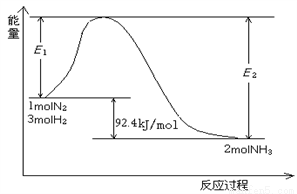
���ڷ�Ӧ��ϵ�м����������Ӧ��������E2�ı仯�ǣ�______________�������������С�����䡱����
�ڽ�һ������N2(g)��H2(g)����2L���ܱ������У���500�桢2��107Pa�·������·�Ӧ��
5���Ӻ�ﵽƽ�⣬���N2Ϊ0.2 mol��H2Ϊ0.6 mol��NH3Ϊ0.2 mol��������ƽ����Ӧ����v(N2)��_______________��H2��ת����Ϊ_______________���÷�Ӧ�ڴ��¶��µĻ�ѧƽ�ⳣ��Ϊ_______________���������ձ���С�����һλ��
������ߢ�������H2��ת���ʣ����д�ʩ���е���____________��
A���������а�ԭ�����ٳ���ԭ����
B�����������ٳ����������
C���ı䷴Ӧ�Ĵ���
D��Һ��������������
��2��1998��ϣ������ʿ��´�ѧ����λ��ѧ�Ҳ��ø����ӵ����Ե�SCY�մɣ��ܴ���H+�����Ӷ�ʵ���˸�ת���ʵĵ�ⷨ�ϳɰ�����ʵ��װ����ͼ��ʾ�������ĵ缫��ӦʽΪ_____________________��
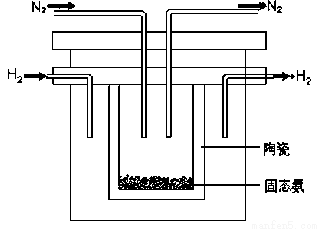
��3���������¡��˹��̵������о��������ڳ��¡���ѹ�����������£�N2�ڴ�������������Fe2O3��TiO2��������ˮ�������з�Ӧ��
2N2(g) +6H2O(l)  4NH3(g) +3O2(g) ��H = a kJ/mol
4NH3(g) +3O2(g) ��H = a kJ/mol
��һ���о�NH3���������¶ȹ�ϵ����ѹ�´ﵽƽ��ʱ��ò���ʵ���������£�
T/K | 303 | 313 | 323 |
NH3������/��10��6mol�� | 4.8 | 5.9 | 6.0 |
�˺ϳɷ�Ӧ��a_________0��������ڡ�����С�ڡ����ڡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡĵ�����и߶���ѧ�ڿ�ѧ��⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������Һ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��
Na2S2O3 + H2SO4 = Na2SO4 + SO2 + S�� + H2O
���и���ʵ�������ȳ��ֻ��ǵ���
ʵ�� | ��Ӧ�¶�/�� | Na2S2O3��Һ | ϡH2SO4 | H2O | ||
V/mL | c/(mol��L-1) | V/mL | c/(mol��) | V/mL | ||
A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡĵ�����и߶���ѧ�ڿ�ѧ��⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A. ���ࡢ��֬�������ʶ��Ǹ߷��ӻ��������ˮ������ղ��ﲻ��ͬ
B. �ڼ�������Һ�зֱ���뱥��Na2SO4��CuSO4��Һ��������������������
C. ������֬�ļ���ˮ�����Ʊ���������
D. �Ҵ������Ͷ��ǿ�������Դ������Ҫ������չ���Ҵ����͡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ����2���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Ժ��ֱ�����ϣ����������ֻ������ͬʱͨ������ı���Һ�У�һ���ܲ�������������ǣ�������
��� | �� | �� | �� |
�� | CO2 | SO2 | ʯ��ˮ |
�� | HCl | CO2 | ʯ��ˮ |
�� | CO2 | SO2 | Ba��NO3��2 |
�� | NO2 | SO2 | BaCl2 |
�� | CO2 | NH3 | CaCl2 |
A. �ڢۢ� B. �ڢۢܢ� C. �٢ۢ� D. �٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡ�����и߶���ѧ����ĩѧ���϶�����B����ѧ�Ծ��������棩 ���ͣ�ѡ����
�������Һ����������֮�������й��ڵ������Һ����������ȷ����(����)
A. 0.1mol•L��1Na2CO3��Һ�У�[OH��]=[HCO3��]+[H+]+[H2CO3]
B. 0.1mol•L��1CH3COONa��Һ�У�[Na+]=[CH3COO��]+[OH��]
C. CH3COONa��NaOH��Na2CO3������Һ��pH��ͬ����Ũ�ȴ�С˳��c ��NaOH����c ��Na2CO3����c��CH3COONa��
D. ��0.1mol•L��1CH3COOH��Һ�еμ�NaOH��Һ�����ԣ���Һ������Ũ�ȵĹ�ϵ��[CH3COO��]��[Na+]��[OH��]=[H+]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʡ����ɽ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
(1)��CH4����ԭNOx�������������������Ⱦ�����磺
CH4(g)��4NO2(g)===4NO(g)��CO2(g)��2H2O(g)�� ��H����574 kJ��mol��1
CH4(g)��4NO(g)===2N2(g)��CO2(g)��2H2O(g) ��H����1 160 kJ��mol��1
���ñ�״����4.48 L CH4��ԭNO2����N2����Ӧ��ת�Ƶĵ�������Ϊ________ (�����ӵ�������NA��ʾ)���ų�������Ϊ________kJ��
(2)��֪��C3H8(g) == CH4(g)��HC��CH(g)��H2(g)����H1����156.6 kJ��mol��1
CH3CH=CH2(g) == CH4(g)��HC��CH(g) ��H2����32.4 kJ��mol��1
����ͬ�����£���ӦC3H8(g) === CH3CH=CH2(g)��H2(g)�Ħ�H��______kJ��mol��1��
(3)�����ڸ�������ˮ������Ӧ�ķ���ʽΪCH4(g)��H2O(g)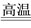 CO(g)��3H2(g)���������ʵ�ȼ�����������±�����֪1 mol H2O(g)ת��Ϊ1 mol H2O(l)ʱ�ų�44.0 kJ������д��CH4��H2O�ڸ����·�Ӧ���Ȼ�ѧ����ʽ�� _______________________________��
CO(g)��3H2(g)���������ʵ�ȼ�����������±�����֪1 mol H2O(g)ת��Ϊ1 mol H2O(l)ʱ�ų�44.0 kJ������д��CH4��H2O�ڸ����·�Ӧ���Ȼ�ѧ����ʽ�� _______________________________��
���� | ȼ����(kJ��mol��1) |
H2(g) | ��285.8 |
CO(g) | ��283.0 |
CH4(g) | ��890.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡĵ�����и�һ��ѧ�ڿ�ѧ��⻯ѧ�Ծ��������棩 ���ͣ������
��1��ʵ���������Ľ����Ʊ�����___________�У�ȡ��ʱ�õ�����������Ʒ��С��������Ƭ����ֽ��____________, ʣ�����Ӧ_______________����һС����Ͷ�뵽����ͭ��Һ�У���Ӧ�����ӷ���ʽΪ______________________________________���۲쵽������Ϊ_____________(��д���)��
a���Ƹ���Һ�����Ĵ��ζ� b�����ڳ���һ��������С��
c����Һ������ɫ�������� d����Һ���к�ɫ��������
��2��ʵ�����������Ļ�ѧ��Ӧ����ʽΪ_________________________________������Ϊ�ж����壬��������������Һ����β������������ɸ����ӷ���ʽ____________�� ��ԭ���������ڹ�ҵ��______________��
��3���������ʼ��������ᷴӦ���������ռ���Һ��Ӧ����________________________________
a. Al b. Mg c. CH3COONH4 d. NaHCO3 e. Al2O3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com