
【题目】A、B、C、D均为中学化学中的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去): A ![]() B
B ![]() C
C ![]() D
D
(1)若A能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的石蕊试纸变红,则C为(填化学式).写出A→B的化学反应方程式: .
(2)若B能使品红溶液褪色,则D的化学式为 . 下列有关B的说法中正确的是(填序号). a.燃烧化石燃料不会产生B
b.造纸过程中可用B漂白纸浆
c.紫色石蕊试液遇B的水溶液会变红
d.可在葡萄糖中添加大量B作杀菌剂
(3)若A为活泼金属元素的单质,C为淡黄色固体,则B的化学式为;写出C→D的离子反应方程式: .
【答案】
(1)NO2;4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
(2)H2SO4; bc
(3)Na2O;2Na2O2+2H2O=4Na++4OH﹣+O2↑
【解析】解:(1)若A的水溶液能使湿润的红色石蕊试纸变蓝,则A是NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,为酸,氨气被氧化生成NO,NO被氧气氧化生成NO2,所以B是NO、C是NO2、D是HNO3,在加热催化剂条件下、氨气被氧化生成NO和水,所以A→B的化学反应方程式为4NH3+5O2 ![]() 4NO+6H2O,
4NO+6H2O,
所以答案是:NO2;4NH3+5O2 ![]() 4NO+6H2O;(2)若B能使品红溶液褪色,则B为SO2,C是SO3、D是H2SO4;
4NO+6H2O;(2)若B能使品红溶液褪色,则B为SO2,C是SO3、D是H2SO4;
a.化石燃料含S元素,燃烧会产生SO2,故错误;
b.SO2具有漂白性,可以在造纸过程中漂白纸浆,故正确;
c.SO2的水溶液显酸性,SO2具有漂白性但不能漂白紫色石蕊试液,所以紫色石蕊试液遇SO2的水溶液会变红,故正确;
d.SO2有毒,所以不可在葡萄糖中添加大量SO2作杀菌剂,故错误;
所以答案是:H2SO4;bc;(3)若A为活泼金属元素的单质,C为淡黄色固体即Na2O2,故A为Na,B为Na2O,D为NaOH,Na2O2与水反应生成氢氧化钠与氧气,反应离子方程式为:2Na2O2+2H2O=4Na++4OH﹣+O2↑.
所以答案是:Na2O;2Na2O2+2H2O=4Na++4OH﹣+O2↑.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2 . 已知该反应中H2O2只发生如下过程:H2O2→O2 . 请回答:
(1)该反应中的还原剂是;
(2)该反应中发生还原反应的是
(3)写出该反应的化学方程式,并标出电子转移的方向和数目: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在乙醇发生的各种反应中,断键方式不正确的是( ) 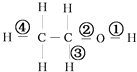
A.与钠反应①
B.在铜催化下加热①③
C.在浓硫酸170°C条件下加热②③
D.与HCl反应生成氯乙烷②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组制取氯气并进行氯气的性质实验,其装置如图所示,请回答下列问题: 
(1)仪器A的名称是 . 实验中制备氯气的反应方程式为 .
(2)C中发生反应的化学方程式为 . 若将干燥的有色布条放入C中,观察到的现象是 , 原因是 .
(3)实验中观察到D溶液变蓝色,查资料得知淀粉碘化钾溶液是淀粉和碘化钾(KI)的混合溶液,写出D装置中发生反应的离子方程式 .
(4)F中氯气与铁粉反应制备无水三氯化铁,查资料知该化合物呈棕红色、易吸水潮解,100℃左右时升华.双通管F中玻璃纤维(不参与反应)的作用是;在F和H装置之间安装G装置的目的是 .
(5)H中NaOH溶液的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中的实验装置可用于制取乙炔.请填空: 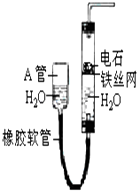
(1)图中,A管的作用是制取乙炔的化学方程式是:
(2)乙炔通入KMnO4酸性溶液中观察到的现象是 , 乙炔发生了反应.
(3)乙炔通入溴的CCl4溶液中观察到的现象是 , 乙炔发生了反应.
(4)为了安全,点燃乙炔前应 , 乙炔燃烧时的实验现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A,B只可能为烃或烃的含氧衍生物,等物质的量的A和B完全燃烧时,消耗氧气的量相等,则A和B的分子量相差不可能为(n为正整数)( )
A.8n
B.14n
C.18n
D.44n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的自然科学. 某同学需要配制0.1molL﹣1 的NaHCO3溶液500mL,请根据溶液配制过程中的情况回答下列问题:
(1)NaHCO3的俗称;配制0.1molL﹣1 的NaHCO3溶液时,应称取固体NaHCO3的质量为 .
(2)实验中除了托盘天平(带砝码和镊子)、烧杯、药匙、玻璃棒外还需要的其它仪器有;其中两次用到玻璃棒,其作用分别是 .
(3)定容观察液面时俯视刻度线,所配溶液浓度(填“偏高”、“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列有关对该溶液的判断不正确的是( ) 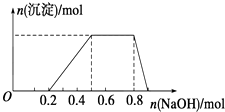
A.该溶液中肯定含有的离子是H+、NH4+、Al3+、SO42﹣
B.肯定不含的阳离子是Mg2+、Fe3+
C.要确定该溶液是否含有Na+ , 必须做焰色反应实验,看焰色是否为黄色
D.该溶液中肯定含有的离子的物质的量之比为n(H+):n(NH4+):n(Al3+):n(SO42﹣)=2:3:1:4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com