
 2Z2,下图是反应过程中,反应速率(v)与时间(t)的关系曲线,下列叙述正确的是
2Z2,下图是反应过程中,反应速率(v)与时间(t)的关系曲线,下列叙述正确的是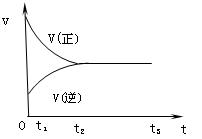
| A.0~t1时,X2、Y2、Z2的物质的量浓度由于反应进行而减小 |
| B.t2~t3时,反应体系中Y2的浓度没有变化 |
| C.到t3以后,反应已达限度,不管如何改变条件,反应不再进行 |
| D.从关系曲线可知,反应开始时体系中只有X2和Y2 |
 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源:不详 题型:填空题
 3C(s)+4D(g)。在高温下达到平衡,测得混合气体中D的浓度为0.3mol·L-1。
3C(s)+4D(g)。在高温下达到平衡,测得混合气体中D的浓度为0.3mol·L-1。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
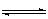 2NH3 (g) (正反应为放热反应)
2NH3 (g) (正反应为放热反应)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
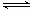 2NO(g)+O2(g)
2NO(g)+O2(g) 2NO(g)+O2(g)体系中,n (NO2)随时间的变化如表:
2NO(g)+O2(g)体系中,n (NO2)随时间的变化如表: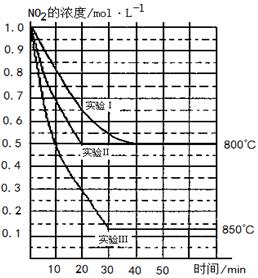
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。 | | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
 CH3OH(g)+ H2O(g)。2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L。下列判断不正确的是 。
CH3OH(g)+ H2O(g)。2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L。下列判断不正确的是 。
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
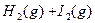

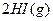 已达到平衡。将活塞外拉,则:
已达到平衡。将活塞外拉,则:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
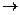 2NH3,当反应达到平衡时,其反应速率可以分别用V(H2),V(N2),V(NH3)表示,则正确的关系式是
2NH3,当反应达到平衡时,其反应速率可以分别用V(H2),V(N2),V(NH3)表示,则正确的关系式是| A.v(H2)="v(N2)=v(NH3)" | B.v(H2)=3v(N2) |
| C.v(NH3)="3(H2)" | D.v(N2)=3V(H2) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO(g)+H2(g);△H>0,下列说法正确的是( )
CO(g)+H2(g);△H>0,下列说法正确的是( ) | A.达到平衡时,反应物的浓度和生成物的浓度相等 |
| B.达到平衡时,反应物和生成物的浓度不随时间的变化而变化 |
| C.由于反应前后分子数相等,所以增加压力对平衡没有影响 |
| D.加入正催化剂可以加快反应达到平衡的速度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.当可逆反应达到平衡状态时,v正= v逆= 0 |
| B.当可逆反应达到平衡状态时,每种成分的质量分数保持不变 |
| C.对于已达平衡的可逆反应,延长反应时间能提高反应物的转化率 |
| D.对于已达平衡的可逆反应,改变外界条件时其平衡状态不会改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com