
【题目】一氧化二氯(Cl2O)是一种常用的氯化剂。常温下,Cl2O是棕黄色、有刺激性气味的气体,熔点为-120.6℃,沸点为2.0℃,易与水反应生成次氯酸。实验室欲用氯气通入含水8%的碳酸钠固体中制备并收集少量纯净的Cl2O,请用下列装置设计实验并探究相关物质的性质。
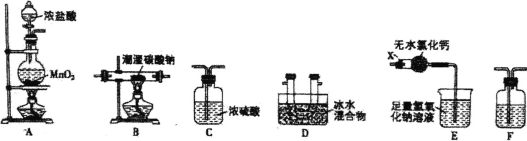
(1)装置E中仪器X的名称为_________。
(2)装置的连接顺序是A_______(每个装置限用一次)。
(3)装置F中盛装试剂的名称为_____,装置E中无水氯化钙的作用是_____。
(4)装置B残留固体中除NaCl外还含有一种酸式盐M,写出装置B中发生反应的化学方程式_____________。
(5)测定残留固体中M的质量分数:取m g样品加适量蒸馏水使之溶解,加入几滴酚酞,用0.1 mol/L的盐酸标准溶液滴定至溶液由红色变为无色,消耗盐酸V1 mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸V2 mL。
①实验时用到的玻璃仪器有烧杯、胶头滴管、玻璃棒、锥形瓶、___。
②求残留固体中M的质量分数___(用含m、V1和V2的代数式表示)。
③若用甲基橙作指示剂滴定结束时,滴定管尖头有气泡,测定结果将填_____(“偏高"、“偏低”或“不变”)。
【答案】干燥管 FBCDE 饱和食盐水 防止E中的水进入D中发生反应 2Na2CO3+H2O+2Cl2![]() 2NaCl+2NaHCO3+Cl2O 酸式滴定管
2NaCl+2NaHCO3+Cl2O 酸式滴定管 ![]() ×100% 偏低
×100% 偏低
【解析】
利用A装置发生反应制取Cl2,由于浓盐酸具有挥发性,制取的氯气中混有杂质HCl,为防止干扰Cl2O的制取,需要先用装置F除去HCl杂质,再利用装置B发生反应2Na2CO3+H2O+2Cl2![]() 2NaCl+2NaHCO3+Cl2O制取Cl2O,由于Cl2O易溶于水,同时与水反应生成次氯酸,所以收集前要通过C装置干燥,再利用装置D收集Cl2O,并验证其沸点低、易液化的特点,同时由于氯气、Cl2O都是大气污染物,最后要用E装置进行尾气处理,以此来解答。
2NaCl+2NaHCO3+Cl2O制取Cl2O,由于Cl2O易溶于水,同时与水反应生成次氯酸,所以收集前要通过C装置干燥,再利用装置D收集Cl2O,并验证其沸点低、易液化的特点,同时由于氯气、Cl2O都是大气污染物,最后要用E装置进行尾气处理,以此来解答。
(1)根据装置图可知装置E中仪器X的名称为干燥管;
(2)A装置制取氯气,由于浓盐酸具有挥发性,所以制取的氯气中混有杂质HCl,为防止干扰Cl2O的制取,需要先用盛有饱和NaCl的水溶液的装置F除去杂质HCl气体,再利用装置B制取Cl2O。Cl2O易溶于水,同时与水反应生成次氯酸,所以收集前要通过盛有浓硫酸的C装置干燥气体,再利用装置D收集Cl2O,并验证其沸点低、易液化的特点,同时由于氯气、Cl2O都是大气污染物,最后要用E装置进行尾气处理,则按气体从左至右流动装置连接顺序是AFBCDE;
(3)装置F中盛装试剂的名称为饱和食盐水,可除去氯气中的HCl,装置E中无水氯化钙的作用是防止E中的水进入D中发生反应;
(4)装置B中反应制取Cl2O,发生反应的化学方程式为2Na2CO3+H2O+2Cl2![]() 2NaCl+2NaHCO3+Cl2O;
2NaCl+2NaHCO3+Cl2O;
(5)①采用滴定方法,用盐酸标准溶液测定待测溶液的浓度,用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、锥形瓶及酸式滴定管;
②滴加盐酸发生CO32-+H+=HCO3-、HCO3-+H+=CO2↑+H2O,残留固体中M的质量分数为![]() ×100%;
×100%;
③用甲基橙作指示剂滴定结束时,滴定管尖头有气泡,则V2偏小,导致测定结果将偏低。


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】某同学在实验室进行铁盐与亚铁盐相互转化实验。
实验I:将Fe3+转化为Fe2+
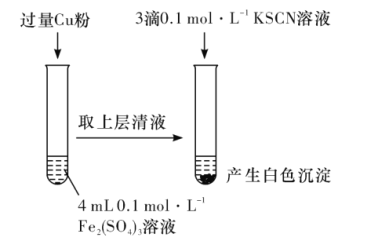
(1)Fe3+与Cu粉发生反应的离子方程式为__。
(2)探究白色沉淀产生的原因,请填写实验方案:__、__。
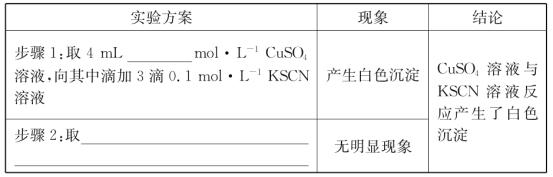
查阅资料:
已知:①SCN-的化学性质与I-相似。
②2Cu2++4I-=2CuI↓十I2。
则Cu2+与SCN-反应的离子方程式为__。
实验II:将Fe2+转化为Fe3+
探究上述现象出现的原因:
查阅资料:Fe2++NO![]() Fe(NO)2+(棕色)
Fe(NO)2+(棕色)
(3)用离子方程式解释NO产生的原因:__。
(4)从化学反应速率与限度的角度对体系中存在的反应进行
反应I:Fe2+与HNO3反应,
反应II:Fe2+与NO反应。
①依据实验现象,可推知反应I的速率比反应II__(填“快"或“慢”)。
②反应I是一个不可逆反应,设计实验方案加以证明___。
③请用化学平衡移动原理解释溶液由棕色变为黄色的原因:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)(题文)8羟基喹啉被广泛用作金属离子的络合剂和萃取剂,也是重要的医药中间体。下图是8羟基喹啉的合成路线。

已知:i. 
ii.同一个碳原子上连有2个羟基的分子不稳定。
(1)按官能团分类,A的类别是__________。
(2)A→B的化学方程式是____________________。
(3)C可能的结构简式是__________。
(4)C→D所需的试剂a是__________。
(5)D→E的化学方程式是__________。
(6)F→G的反应类型是__________。
(7)将下列K→L的流程图补充完整:____________

(8)合成8羟基喹啉时,L发生了__________(填“氧化”或“还原”)反应,反应时还生成了水,则L与G物质的量之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,直线交点处的圆圈为NaCl晶体中Na+或Cl-所处的位置。这两种离子在空间三个互相垂直的方向上都是等距离排列的。
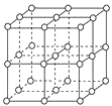
(1)请将其中代表Na+的圆圈涂黑(不必考虑体积大小),以完成NaCl晶体结构示意图______________。
(2)晶体中,在每个Na+的周围与它最接近的且距离相等的Na+共有________个。
(3)在NaCl晶胞中正六面体的顶角上、面上、棱上的Na+或Cl-为该晶胞与其相邻的晶胞所共有,一个晶胞中Cl-的个数等于________,即________(填计算式);Na+的个数等于________,即________(填计算式)。
(4)设NaCl的摩尔质量为Mrg·mol-1,食盐晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA。食盐晶体中两个距离最近的钠离子间的距离为____________________________________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度T1和T2时,分别将0.50 mol CH4和1.20 mol NO2充入体积为1 L的密闭容器中,发生如下反应:CH4(g)+2NO2(g) ![]() N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
时间/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | …… | 0.15 |
下列说法正确的是( )
A.该反应的ΔH>0、T1<T2
B.T2时CH4的平衡转化率为30.0%
C.T2时40min后,断裂4mol C-H键同时断裂4 mol O-H键
D.T1时向平衡体系中再充入CH4,建立平衡后CO2的体积分数一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰电池(俗称干电池)在生活中的用量很大。其中普通锌锰电池的构造图如右图所示。回答下列问题:
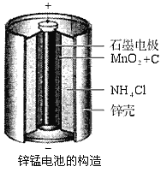
(1)电池放电时发生的主要反应为:
Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH,正极发生的主要反应是________________________。
(2)下图表示从废旧普通锌锰电池除去锌壳和电极后的内容物中回收制备KMnO4等物质的一种工艺(不考虑废旧电池中实际存在的少量其他金属)。

①黑色固体混合物水浸时为提高浸出速率,常采用的措施为________________(答两条);得到滤液加入稀盐酸的作用为__________________。
②滤渣水洗灼烧后固体主要成份只有一种,操作a中得到熔块的主要成分是K2MnO4,该过程中发生反应的化学方程式为:_____________________________。
③图中产物的化学式分别为:A__________、B_________。
(3)准确称量得到的KMnO4(不含能与草酸反应的杂质)3.160 g,放入小烧杯中,加水溶解后转移到200mL容量瓶中定容,在锥形瓶中用差量法称取0.6700 g无水草酸钠,加入足量硫酸溶液溶解,加热至75~80℃。用已配制好的KMnO4溶液进行滴定,消耗溶液体积为22.50mL。
已知Mr(Na2C2O4)=134 Mr(KMnO4)=158
①判断滴定终点的现象是__________________。
②KMnO4的纯度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】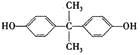 双酚A是一种重要的化工原料,它的一种合成路线如下图所示:
双酚A是一种重要的化工原料,它的一种合成路线如下图所示:
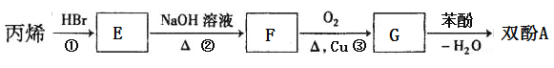 下列说法正确的是
下列说法正确的是
A. 1mol双酚A最多可与2molBr2反应
B. G物质是乙醛的同系物
C. E物质的名称是1-溴丙烷
D. 反应③的化学方程式是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15 分)化合物H 是合成药物盐酸沙格雷酯的重要中间体,其合成路线如下:
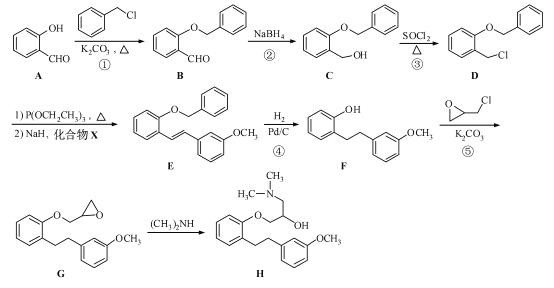
(1)化合物A 中的含氧官能团为 和 (填官能团名称)。
(2)反应①→⑤中,属于取代反应的是 (填序号)。
(3)写出同时满足下列条件的B 的一种同分异构体的结构简式: 。
I. 分子中含有两个苯环;II. 分子中有7 种不同化学环境的氢;III. 不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应。
(4)实现D→E 的转化中,加入的化合物X 能发生银镜反应,X 的结构简式为 。
(5)已知:![]() 。化合物
。化合物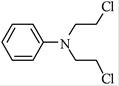 是合成抗癌药物美法伦的中间体,请写出以
是合成抗癌药物美法伦的中间体,请写出以![]() 和
和![]() 为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用碳-碳偶联反应合成新物质是有机合成的研究热点之一,如:

化合物Ⅰ可以由以下合成路线获得:
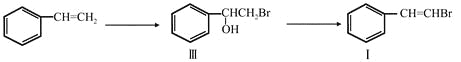
(1)化合物Ⅰ的分子式为__________________。
(2)化合物Ⅱ与溴的CCl4溶液发生加成反应,产物的结构简式为______________________。
(3)化合物Ⅲ生成化合物Ⅰ的化学方程式为_____________;(注明反应条件)化合物Ⅲ与NaOH水溶液共热的化学方程式为_____________。(注明反应条件)
(4)化合物Ⅳ是化合物Ⅲ的一种同分异构体,其苯环上只有一种取代基,Ⅳ的催化氧化产物Ⅴ能发生银镜反应。Ⅳ的结构简式为_____________,Ⅴ的结构简式为_____________。
(5)有机物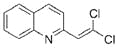 与BrMgCH2(CH2)3CH2MgBr在一定条件下发生类似反应①的反应,生成的有机化合物Ⅵ(分子式为C16H17N)的结构简式为____________________。
与BrMgCH2(CH2)3CH2MgBr在一定条件下发生类似反应①的反应,生成的有机化合物Ⅵ(分子式为C16H17N)的结构简式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com