
据报道,锌电池可能将会取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染。其电池反应为2Zn+O2===2ZnO,原料为锌粒、电解液和空气。则下列叙述正确的是( )
A.锌为正极,空气进入负极反应
B.负极反应为Zn-2e-===Zn2+
C.正极发生氧化反应
D.电解液为强酸
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
在原电池和电解池的电极上所发生的反应,同属氧化反应的是( )
A.原电池的正极和电解池的阳极所发生的反应
B.原电池的正极和电解池的阴极所发生的反应
C.原电池的负极和电解池的阳极所发生的反应
D.原电池的负极和电解池的阴极所发生的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知空气—锌电池的电极反应为:锌片:Zn+2OH--2e-===ZnO+H2O;碳棒:O2+2H2O+4e-===4OH-,据此判断,锌片是( )
A.正极,被还原 B.正极,被氧化
C.负极,被还原 D.负极,被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.水果电池是高效环保的家用电池
B.燃料电池是一种高效但是会污染环境的新型电池
C.化学电源的反应基础是氧化还原反应
D.手机上用的锂离子电池属于一次电池
查看答案和解析>>
科目:高中化学 来源: 题型:
燃料电池是目前正在探索的一种新型电池。它主要是利用燃料在燃烧过程中把化学能直接转化为电能,目前已经使用的氢氧燃料电池的基本反应是
x极:O2(气)+2H2O(液)+4e-===4OH-
y极:H2(气)+2OH--2e-===2H2O(液)
回答下列问题:
(1)x是________极,发生________反应。(填“氧化”或“还原”,下同)
(2)y是________极,发生________反应。
总反应方程式为______________________________________。
(3)若反应后得到5.4 g液态水,此时氢氧燃料电池转移的电子数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某容器中充入H2和N2,在一定条件下合成NH3,下列叙述不正确的是( )
A.开始反应时,正反应的速率最大
B.随着反应的进行,正反应的速率逐渐减小,最终减小为零
C.随着反应的进行,逆反应的速率逐渐增大,后保持不变
D.随着反应的进行,正反应的速率逐渐减小,最终与逆反应的速率相等且保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时,表明反应:A(g)+B(g)C(g)+D(g)已达平衡的是( )
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.气体的总物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
将N2、H2的混合气体分别充入甲、乙、丙三个容器后,测得反应速率分别为甲:v(H2)=3 mol/(L·min);乙:v(N2)=2 mol/(L·min);丙:v(NH3)=1 mol/(L·min)。则三个容器中合成氨的速率( )
A.v(甲)>v(乙)>v(丙) B.v(乙)>v(丙)>v(甲)
C.v(丙)>v(甲)>v(乙) D.v(乙)>v(甲)>v(丙)
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有__________________。
(2)硫酸铜溶液可以加快氢气生成速率的原因是____________。
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________。
(4)要加快上述实验中气体产生的速率,还可采取的措施有________________________________________________________(答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
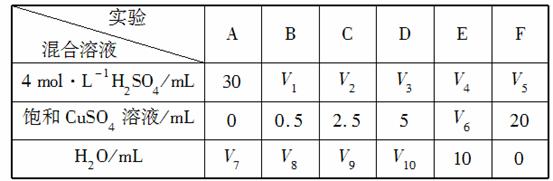
①请完成此实验设计,其中:V1=________,V6=________,V9=________;
②反应一段时间后,实验A中的金属呈________色,实验E中的金属呈________色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
___________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com