
将0.48 g Mg粉加入到500 mL 0.1 mol·L-1的硝酸中恰好完全反应,则还原产物可能是 ( )。
A.NO2 B.NO
C.N2O3 D.NH
科目:高中化学 来源: 题型:
下列关于淀粉和纤维素的叙述中,不正确的是( )
A.它们都是混合物
B.它们都是天然高分子化合物
C.它们是同分异构体
D.它们水解的最终产物都是葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,反应A2(g)+B2(g)
 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )
A.单位时间内生成n mol的A2,同时生成n mol的AB
B.容器内的总压强不随时间的变化而变化
C.单位时间内生成2n mol的AB同时生成n mol的B2
D.平均相对分子质量不随时间变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
现有部分前36号元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| R | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
| S | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| T | 基态原子3d轨道上有1个电子 |
| X |
|
(1)R元素的第一电离能要大于其同周期相邻的元素,原因是_____________。
(2)S元素的常见化合价为________,原因是__________________________。
(3)T元素的原子N能层上电子数为________。
(4)X的核外电子排布图违背了________。用X单质、碱金属盐及碱土金属盐等可以做成焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,化合物M对番茄灰霉菌有较好的抑菌活性,其合成路线如下图所示:

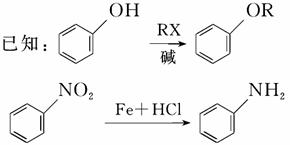
完成下列填空:
(1)写出反应类型:
反应③________;反应④________。
(2)写出结构简式:
A_____________________________________________________________;
E__________________________________________________________。
(3)写出反应②的化学方程式:_______________________________________
_________________________________________________________________。
(4)B的含苯环结构的同分异构体中,有一类能发生碱性水解,写出检验这类同分异构体中的官能团(酚羟基除外)的试剂及出现的现象:
试剂(酚酞除外):___________________________________________;
现象:_____________________________________________________。
(5)写出两种C的含苯环结构且只含4种不同化学环境氢原子的同分异构体的结构简式:
_________________________________________________________
_________________________________________________________。
(6)反应①、反应②的先后次序不能颠倒,请解释原因:_________________
____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在硫酸铁电化浸出黄铜矿精矿工艺中,有一主要反应:CuFeS2+4Fe3+===Cu2++5Fe2++2S,反应结束后,经处理获得单质硫x mol。下列说法正确的是 ( )。
A.反应中硫元素被氧化,所有铁元素均被还原
B.氧化剂是Fe3+,氧化产物是Cu2+
C.反应中转移电子的物质的量为x mol
D.反应结束后,测得溶液中三种金属离子的总物质的量为y mol,则原Fe3+的总物质的量为(y-x) mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.溶度积大的化合物溶解度肯定大
B.向含有AgCl固体的溶液中加入适量的水使AgCl溶解又达到平衡时,AgCl的溶度积不变,其溶解度也不变
C.将难溶电解质放入纯水中,溶解达到平衡时,电解质离子的浓度的乘积就是该物质的溶度积
D.AgCl水溶液的导电性很弱,所以AgCl为弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是 ( )
A.向水中通入氯气:Cl2+H2O=2H++Cl-+ClO-
B.向氯化铁溶液中加入铜:2Fe3++3Cu=2Fe+3Cu2+
|
D.向二氧化锰中滴加浓盐酸并加热:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
生活中下列物质的应用或现象解释错误的是( )
A.食盐可作调味剂,也可作食品防腐剂
B.大量燃烧化石燃料是造成雾霾天气的重要因素之一
C.装饰材料释放的甲醛会造成空气污染
D.磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com