
| A. | 8.3 | B. | 8.7 | C. | 9 | D. | 9.7 |
分析 由pH计算c(OH-),结合Kw=c(H+)×c(OH-)计算c(H+),根据pH=-lgc(H+)计算.
解答 解:将pH=8和pH=10的两强碱溶液等体积混合,则混合后c(OH-)=$\frac{1{0}^{-6}mol/L+1{0}^{-4}mol/L}{2}$≈$\frac{1}{2}$×10-4mol/L,
则c(H+)=$\frac{1×1{0}^{-14}}{\frac{1}{2}×1{0}^{-4}}$=2×10-10mol/L,
pH=-lgc(H+)≈9.7,
故选D.
点评 本题考查溶液pH的计算,侧重于学生的分析、计算能力的考查,注意把握计算的思路以及相关计算公式的运用,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧根离子的电子式是 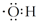 | |
| B. | 二氧化碳分子的比例模型是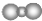 | |
| C. | 芳香烃的组成通式是CnH2n-6(n≥6) | |
| D. | 12C和14C的原子结构示意图均可表示为 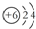 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高一阶段考一化学卷(解析版) 题型:选择题
根据反应式:2Fe3++2I﹣═2Fe2++I2,Br2+2Fe2+═2Br﹣+2Fe3+,可以判断微粒的氧化性从强到弱的顺序是( )
A.Fe3+、Br2、I2 B.I2、Br2、Fe3+ C.Br2、Fe3+、I2 D.Br2、I2、Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒半径:S<S2-<K | B. | 稳定性:H2O>H2S>PH3 | ||
| C. | 酸性:H3PO4<HNO3<HClO4 | D. | 沸点:HF<HCl<HBr<HI |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素非金属性:逐渐减弱 | B. | 单质氧化性:逐渐减弱 | ||
| C. | 氢化物稳定性:逐渐增强 | D. | 最高价含氧酸酸性:逐渐减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com