
| A. | A与D可形成含18e-的离子化合物 | |
| B. | B单质在C单质中燃烧生成原子个数比为1:1的化合物 | |
| C. | D的氧化物为酸性氧化物,溶于水可制得D的含氧酸 | |
| D. | D与E组成的化合物中,各原子最外层均达到8电子结构 |
分析 短周期元素A、B、C、D、E的原子序数依次增大,A的一种同位素的质量数为1,则A为氢元素;
C原子的最外层电子数是电子层数的3倍,则C原子有2个电子层,最外层电子数为6,则C为氧元素;
A和B同主族,B原子序数小于氧元素,则B为Li元素;
D的最高正价与最低负价的绝对值相等,次外层电子数为4,处于ⅣA族,原子序数大于氧元素,故D为Si元素;
E的最高价氧化物的水化物的化学式为HnEO2n+2,令E元素化合价为x,则n+x=4n+4,即x=3n+4,故x=7,则E为Cl元素,据此解答.
解答 解:短周期元素A、B、C、D、E的原子序数依次增大,A的一种同位素的质量数为1,则A为氢元素;
C原子的最外层电子数是电子层数的3倍,则C原子有2个电子层,最外层电子数为6,则C为氧元素;
A和B同主族,B原子序数小于氧元素,则B为Li元素;
D的最高正价与最低负价的绝对值相等,次外层电子数为4,处于ⅣA族,原子序数大于氧元素,故D为Si元素;
E的最高价氧化物的水化物的化学式为HnEO2n+2,令E元素化合价为x,
则n+x=4n+4,
即x=3n+4,
故x=7,
则E为Cl元素,
A.硅化氢是共价化合物,故A错误;
B.Li在氧气中燃烧生成Li2O,故B错误;
C.二氧化硅属于酸性氧化物,不能溶于水,故C错误;
D.Si与Cl组成的化合物为SiCl4,分子中Si原子与Cl之间形成1对共用电子对,各原子最外层均达到8电子稳定结构,故D正确;
故选:D.
点评 本题考查结构性质位置关系应用,难度不大,推断元素是解题关键,侧重对基础知识的巩固.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:解答题
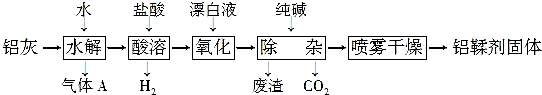
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
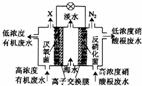 一种三室微生物燃料电池污水净化系统原理如图所示,图中废水有机物可用 C6H10O5表示.下列有关该燃料电池的说法错误的是( )
一种三室微生物燃料电池污水净化系统原理如图所示,图中废水有机物可用 C6H10O5表示.下列有关该燃料电池的说法错误的是( )| A. | 中间室中的 Cl-向左室移动 | |
| B. | 左、右两室溶液混合后所得溶液的酸性:反应前<反应后 | |
| C. | X气体为CO2 | |
| D. | 左边离子交换膜为阴离子交換膜,右边离子交换膜为阳离子交換膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S>O>F | B. | S2->Cl->K+>Ca2+ | C. | F->O2->Na+>Mg2+ | D. | Fe>Fe2+>Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
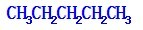 ;
;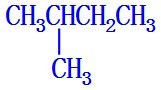 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向无水乙醇中加入浓H2SO4,加热至170℃,将产生的气体通入酸性KMnO4溶液中紫红色褪去,使溶液褪色的气体一定是乙烯 | |
| B. | 苯酚钠溶液中通入少量二氧化碳得到苯酚和碳酸钠溶液 | |
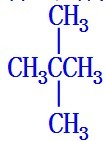
| C. | 正丁烷的所有碳原子都在同一条直线上 | |
| D. | 实验室可用电石与饱和食盐水反应制取乙炔气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
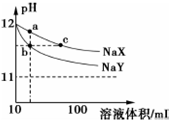 常温下,体积均为10mL、pH均为12的NaX和NaY两种钠盐溶液,分别加水稀释,pH随溶液体积的变化如图所示.下列叙述错误的是( )
常温下,体积均为10mL、pH均为12的NaX和NaY两种钠盐溶液,分别加水稀释,pH随溶液体积的变化如图所示.下列叙述错误的是( )| A. | 相同温度下,电离平衡常K(HX)<K(HY) | |
| B. | b、c两点溶液中水的电离程度相同 | |
| C. | a点溶液中:c(H+)+c(HX)=c(OH-) | |
| D. | b、c两点溶液中Na+的物质的量:nb(Na+)<nc(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M一定是第VIA族元素 | B. | M的最高价氧化物为RO2 | ||
| C. | M的气态氢化物一定能形成氢键 | D. | M的气态氢化物溶于水可能显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | ||||||
| D | E | F | |||||
| C | I | G | H |
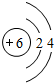
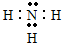
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com