
分析 (一)(1)酸碱中和滴定时,眼睛要注视锥形瓶内溶液的颜色变化;滴定终点时溶液颜色由红色突变为无色;
(2)根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析不当操作对V(标准)×的影响,以此判断浓度的误差;
(二)(3)KMnO4溶液具有强氧化性,应用酸式滴定管;
(4)①根据MnO4-转变成Mn2+溶液颜色有紫色变成无色,现象明显;
②先根据关系式5Fe2+~MnO4-计算出100mL溶液中含有的铁,可求出质量百分数.
解答 解:(1)酸碱中和滴定时,眼睛要注视锥形瓶内溶液的颜色变化,滴定终点时溶液颜色由红色突变为无色,且半分钟内不褪色,
故答案为:锥形瓶中溶液颜色的变化;红色突变为无色;
(2)A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$可知,测定c(NaOH)偏大,故A错误;
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$可知,测定c(NaOH)无影响,故B错误;
C.酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$可知,测定c(NaOH)偏大,故C错误;
D.读取盐酸体积时,滴定结束时俯视读数,造成V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$可知,测定c(NaOH)偏低,故D正确;
故选D;
(二)(3)KMnO4溶液具有强氧化性,准确量取一定体积的KMnO4溶液需要使用的仪器是酸式滴定管,故答案为:酸式滴定管;
(4)①MnO4-转变成Mn2+溶液颜色有紫色变成无色,KMnO4标准溶液在酸性条件下进行氧化还原滴定时,不需要指示剂,
故答案为:否;高锰酸钾溶液有颜色,故不需其他指示剂;
②用关系式法计算:
5Fe2+~MnO4-
4×10-3mol 1.000×10-2mol•L-1×0.02L×4
铁元素的质量为:4×10-3mol×56g/mol=2.24×10-1g,铁元素的质量分数$\frac{2.24×1{0}^{-1}}{5.000}$×100%=4.480%,
故答案为:4.48%.
点评 本题考查物质含量的测定,为高频考点,侧重考查学生的分析能力、实验能力和计算能力的考查,注意把握实验的原理、操作方法以及相关的计算,难度中等.


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:选择题
| A. | FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| B. | 将1mol/L的NaCl溶液保存在容量瓶中 | |
| C. | 凡是给玻璃仪器加热,都要垫石棉网,以防仪器炸裂 | |
| D. | 用pH试纸检验某溶液的酸碱性时,一定要先用蒸馏水湿润 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2LCH4含有5NA个电子 | |
| B. | 标准状况下,22.4L氦气含有2NA个原子 | |
| C. | 常温常压下,22.4L CO2和SO2混合气体含有2NA个氧原子 | |
| D. | 46gNO2和N2O4的混合气体含氮原子数为NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
 ;
;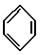 ,常用作有机溶剂.该有机物分子式为 C6H6 ,其中碳元素与氢元素的质量比m(C):m(H)=12:1(相对原子质量:H-1 C-12)
,常用作有机溶剂.该有机物分子式为 C6H6 ,其中碳元素与氢元素的质量比m(C):m(H)=12:1(相对原子质量:H-1 C-12)查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
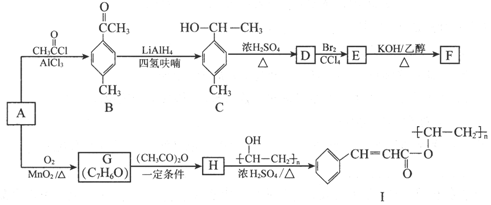
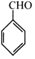
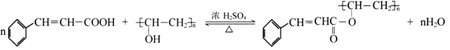
 (写出其中一种的结构简式).
(写出其中一种的结构简式).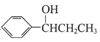 的合成路线
的合成路线 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com