
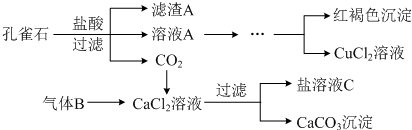
分析 孔雀石的主要成分为Cu2(OH)2CO3,还含少量Fe、Si的化合物,加入稀盐酸反应后生成二氧化碳气体,得到溶液氯化铜溶、氯化亚铁液A,过滤得到二氧化硅固体;然后将Fe2+氧化成Fe3+,再加入CuO固体调节溶液pH沉淀铁离子过滤得到滤液为氯化铜溶液,通过蒸发浓缩,冷却结晶,过滤洗涤得到氯化铜晶体;由工艺流程转化关系可知,应先向CaCl2溶液中加入碱性物质并且不引入新杂质,故气体X应为碱性气体,应为氨气;
(1)孔雀石和盐酸反应生成氯化铜、二氧化碳和水来解答;
(2)过滤得到二氧化硅固体;向CaCl2溶液中加入碱性物质并且不引入新杂质,故气体为氨气;
(3)由溶液制得晶体,应进行蒸发、冷却结晶、过滤等操作;
(4)②根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
②根据盐酸和氢氧化钠的反应,计算出剩余的盐酸的物质的量,用盐酸总的物质的量减去剩余的盐酸的物质的量,就是碳酸钙消耗的盐酸,再计算出碳酸钙的质量分数即可.
解答 解:(1)孔雀石和稀盐酸反应生成氯化铜、二氧化碳和水,反应的离子方程式为:Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O;
故答案为:Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O;
(2)滤渣A成分的化学式是SiO2,气体B的分子式是NH3;
故答案为:SiO2;NH3;
(3)将CuCl2溶液酸化后,经过加热浓缩、冷却结晶、过滤、洗涤、干燥,得到CuCl2•3H2O晶体;
故答案为:加热浓缩;冷却结晶;
(4)①根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知所需的仪器有天平、药匙、烧杯、玻璃棒、250mL容量瓶和胶头滴管,故
所用到的玻璃仪器除烧杯、玻璃棒外还有胶头滴管、250 mL容量瓶;
故答案为:胶头滴管、250 mL容量瓶;
②NaOH+HCl=NaCl+H2O
1 1
CaCO3+2HCl=CaCl2+CO2+H2O
1 2
根据上面两个公式可求得于CaCO3反应的HCl物质的量为(75-15)×0.1/1000=0.006mol,CaCO3的物质的量为:0.003mol,质量0.003mol×100g/mol=0.3g,胃药中碳酸钙的质量分数为$\frac{0.3g}{0.6g}$×100%=50%;
故答案为:50%.
点评 本题以化学工艺流程图为载体,设计方案制备CuCl2•3H2O及CaCO3,考查无机化学与实验的融合能力,以及完成基本实验操作的能力和化学计算,难度大.


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源:2017届广西桂林十八中高三上10月月考化学试卷(解析版) 题型:选择题
某铁的氧化物(FexO)1.52g溶于足量盐酸中,向所得溶液中通入标准状况下112mLCl2,恰好将Fe2+完全氧化。x值为( )
A.0.80 B.0.85 C.0.90 D.0.93
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 浓度为0.06mol/L.
浓度为0.06mol/L.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
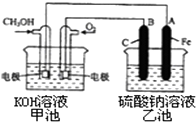 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
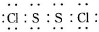 ,它不稳定,在水中易发生岐
,它不稳定,在水中易发生岐| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
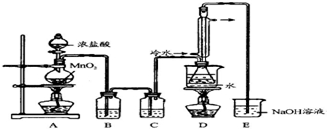
 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com