
| A. | 随着温度的升高,碳酸溶液的pH减小 | |
| B. | 随着温度的升高,纯水的pH减小 | |
| C. | 新氯水制经光照一段时间后,pH减小 | |
| D. | 氢氧化钠溶液久置于空气中,pH增大 |
分析 A.升高温度,碳酸分解,二氧化碳溶解度减小;
B.升高温度,促进水的电离;
C.光照条件下次氯酸分解生成盐酸;
D.氢氧化钠与空气中二氧化碳反应.
解答 解:A.碳酸溶液呈酸性,升高温度,碳酸分解,二氧化碳溶解度减小,碳酸溶液的pH增大,故A错误;
B.升高温度,促进水的电离,溶液氢离子浓度增大,则pH减小,故B正确;
C.光照条件下次氯酸分解生成盐酸,溶液酸性增强,则pH减小,故C正确;
D.氢氧化钠与空气中二氧化碳反应,氢氧化钠溶液浓度降低,则pH减小,故D错误.
故选B.
点评 本题综合考查电解质的离子以及元素化合物知识,为高频考点,侧重考查学生的分析能力,注意把握水的电离特点以及次氯酸的性质,难度不大.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:实验题
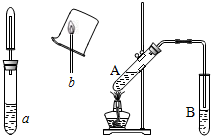 乙醇性质探究
乙醇性质探究查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 手机上用的锂离子电池属于二次电池 | |
| B. | 铜锌原电池工作时,电子从铜电极流向锌电极 | |
| C. | 氢氧燃料电池可把化学能转化为电能 | |
| D. | 锌锰干电池中,锌电极是负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 }及阻燃剂四溴双酚A.合成线路如下:
}及阻燃剂四溴双酚A.合成线路如下: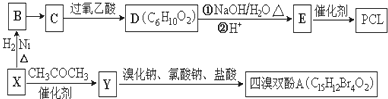
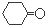

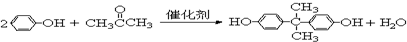 .
.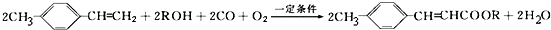
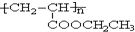 ,写出合成该涂料的反应流程图:
,写出合成该涂料的反应流程图: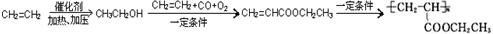 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
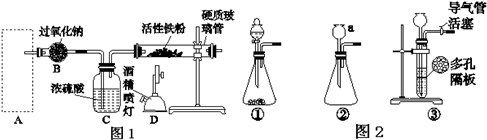
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑦⑧⑨⑩ | B. | ①②③⑤⑧⑨ | C. | ②⑤⑥⑦⑧ | D. | ②④⑦⑧⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | ①能使溴的四氯化碳溶液褪色,常作植物生长调节剂; ②比例模型如图所示:  ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成; ②球棍模型如图所示: 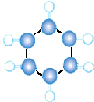 |
| C | ①C、H、O三种元素组成; ②与Na反应产生H2; ③与D反应可生成酯. |
| D | ①C、H、O三种元素组成,是厨房中的常见调味剂; ②水溶液能使紫色石蕊试液变红. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com