
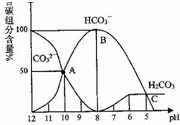
 常温下,某Na2CO3溶液中含有碳组分含量(物质的量分数)随溶液的pH逐渐降低而发生变化如图,下列说法正确的是( )
常温下,某Na2CO3溶液中含有碳组分含量(物质的量分数)随溶液的pH逐渐降低而发生变化如图,下列说法正确的是( )| A. | 在滴有酚酞的Na2CO3溶液中逐滴加盐酸至溶液恰好变为无色,得到溶液 | |
| B. | 有CO2气体放出的范围是pH≤5 | |
| C. | HCO3-的电离平衡常数为1×10-4 | |
| D. | pH=11的Na2CO3溶液稀释到体积为原来的100倍后pH=9 |
分析 A.酚酞变色范围为8-10,酚酞恰好为无色时,pH为8;
B.依据图象可知,当pH在5-6时碳酸达到饱和;
C.依据:K=$\frac{C(H{\;}^{+})C(C{{O}_{3}}^{2}{\;}^{-})}{C(HC{O}_{3}{\;}^{-})}$计算解答;
D.碳酸钠为强碱弱酸盐,稀释时水解程度增大.
解答 解:A.从图象中可知,酚酞恰好为无色时,pH为8,此时应为碳酸氢钠溶液,故A正确;
B.依据图象可知,当pH在5-6时碳酸达到饱和,所以有CO2气体放出的范围是pH≤6,故B错误;
C.从图中数据可知,当pH=10时,碳酸根离子浓度等于碳酸氢根离子浓度,所以K=$\frac{C(H{\;}^{+})C(C{{O}_{3}}^{2}{\;}^{-})}{C(HC{O}_{3}{\;}^{-})}$=C(H+)=10-10,故C错误;
D.碳酸钠为强碱弱酸盐,稀释时水解程度增大,pH=11的Na2CO3溶液稀释到体积为原来的100倍后pH>9,故D错误;
故选:A.
点评 本题考查了碳酸钠、碳酸氢钠的性质,明确图象中各种物质随着pH变化情况是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Fe2+、Na+、Cl-、SCN- | B. | Na+、Cu2+、NO3-、Cl- | ||
| C. | Na+、H+、NO3-、SO42- | D. | Al3+、Na+、Cl-、NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 未用标准液润洗滴定管 | |
| B. | 盛标准液的滴定管尖嘴部分有气泡未排出就开始滴定,滴定后气泡消失 | |
| C. | 锥形瓶用蒸馏水洗,未用待测液润洗 | |
| D. | 振荡时锥形瓶中液滴飞溅出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
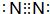 ;B的原子在周期表中的位置是第三周期ⅡA族
;B的原子在周期表中的位置是第三周期ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是某兴趣小组探究不同条件下化学能转变为电能的装置
如图是某兴趣小组探究不同条件下化学能转变为电能的装置查看答案和解析>>
科目:高中化学 来源: 题型:填空题
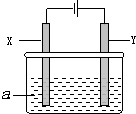
| 方案 | X | Y | a溶液 |
| A | 铁 | 银 | AgNO3 |
| B | 铁 | 银 | Fe(NO3)3 |
| C | 银 | 铁 | AgNO3 |
| D | 银 | 石墨 | AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入适量NaNO3溶液 | B. | 加入适量NaOH溶液 | ||
| C. | 加入适量Na2CO3溶液 | D. | 加入适量NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑥ | B. | ③⑤ | C. | ②③④ | D. | ④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com