
ij��Һ�г���H+��OH�����⣬�����д�����Mg2+��Fe3+��Cl���������������ӵ����ʵ���Ũ��֮��Ϊ1��1��6�������йظ���Һ�ж���ȷ����
A�������Һ�м���KI��Һ��ԭ�е�5�����ӵ����ʵ�������
B�������Һ�еμ�ϡNaOH��Һ���������ְ�ɫ����
C�������Һ�м���������ۣ�ֻ�����û���Ӧ
D������Һ��c (Cl��)=0.6mol/L�������Һ��pH=1
 ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д� ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д� ��У���һ��ͨϵ�д�
��У���һ��ͨϵ�д� �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
ij��ѧ��ȤС��������Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�졷ʵ��ʱ���֣�������Һ����������Һ��Ӧʱ����Һ��ɫ������졣Ϊ��̽���˷�Ӧ������С����ԭ��ͬѧ��������ʵ�顣
��1��0.10mol/L H2C2O4��Һ�����ƣ�
ʵ����������80mL 0.10mol/L H2C2O4 ��Һ����Ҫ��ȡ���ᾧ�壨H2C2O4��2H2O g����ȷ��0.1g����ʵ������Ҫ�õ��IJ����������˲���������ͷ�ιܡ���Ͳ��У� ��������ţ�
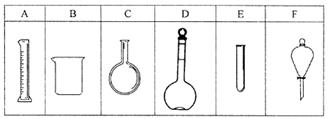
��2����Ӧ���ʱ仯��̽��
| 1���Թ� | 2���Թ� | |
| �����Լ� | 2mL0.10mol/L H2C2O4 ��Һ�� ����ϡ���ᣬ4mL0.010mol/L ��KMnO4��Һ | 2mL0.10mol/L H2C2O4 ��Һ���� ��ϡ���ᣬ4mL0.010mol/L�� KMnO4��Һ������MnSO4���塣 |
| ��ɫʱ�� | 31�� | 4�� |
��H2C2O4��Һ�����Ե�KMnO4��Һ��Ӧ�����ӷ���ʽΪ ��
�ڼ�ͬѧ�ܹ��ó����� ��
��3����һ�������£��ݻ�Ϊ100 L�ܱ������з�����Ӧ��CH4(g)+H20(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
 ��H>0����1��O molCH4��2��O mol H 20(g)ͨ����ܱ�������10 minʱ��O��1 mol CO���ɣ���10 min�ڸ÷�Ӧ��ƽ�����ʦ�(H2) ��
��H>0����1��O molCH4��2��O mol H 20(g)ͨ����ܱ�������10 minʱ��O��1 mol CO���ɣ���10 min�ڸ÷�Ӧ��ƽ�����ʦ�(H2) ��
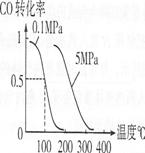
(4)��ѹǿΪO��1 MPa�����£��ݻ�ΪV Lij�ܱ�������amol CO��2amol H2�ڴ��������·�Ӧ���ɼ״���CO(g)+2H2(g)![]() CH3OH(g)��CO��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
CH3OH(g)��CO��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
�ٸ÷�Ӧ��AH O(�<������>����=��)��
��100��ʱ�÷�Ӧ��ƽ�ⳣ��K (�ú�n��V�Ĵ���ʽ��ʾ)��
���������������������£�������a mol CO��2a mol H2���ﵽ��ƽ��ʱ��CO��ת���� (���������С�����䡱)��ƽ�ⳣ�� (���������С�����䡱)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com