
 碳和氮的许多化合物在工农业生产和生活中有重要的作用.
碳和氮的许多化合物在工农业生产和生活中有重要的作用.分析 (1)由已知热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式;
(2)由反应可知,负极上氨气失去电子生成氮气;
(3)因为NH4++H2O?NH3•H2O+H+,pH=5,$\sqrt{0.1×\frac{Kw}{kb}}$=10-5;
(4)①根据反应物和生成物写出化学方程式;
②据题意,根据通入气体判断两极,书写电极反应式;阴离子向负极移动.
解答 解:(1)①2NH3(g)+CO2(g)→NH2CO2 NH4(s)-l59.47kJ•mol-1
②NH2CO2NH4(s)→CO(NH2)2(s)+H2O(g)+116.49kJ•mol-1
③H2O(l)→H2O(g)+88.0kJ•mol-1
依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-130.98KJ/mol;
故答案为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-130.98KJ/mol;
(2)电池反应为:4NH3+3O2=2N2+6H2O.该电池负极是氨气失电子生成氮气,负极的电极反应式为2NH3+6OH--6e-=N2+6H2O,
故答案为:2NH3+6OH--6e-=N2+6H2O;
(3)NH4++H2O?NH3•H2O+H+,pH=5,$\sqrt{0.1×\frac{Kw}{kb}}$=10-5,即Kb=10-5,故答案为:10-5;
(4)①反应物为NH3和NO,发生氧化还原反应,可得到产物为:N2和H2O,化学方程式为:4NH3+6NO$\frac{\underline{\;催化剂\;}}{\;}$5N2+6H2O,
故答案为:4NH3+6NO$\frac{\underline{\;催化剂\;}}{\;}$5N2+6H2O;
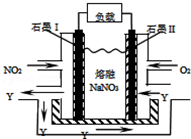
②据题意,通O2一极为正极,电极反应式为O2+2N2O5+4e-=4NO3-;通NO2一极为负极,电极反应为:NO2+NO3--e-=N2O5,阴离子向负极移动,则NO3-向I极移动,即向左侧移动,
故答案为:NO2+NO3--e-=N2O5;左.
点评 本题考查原电池及反应热计算、Kb计算等,综合性较强,为高频考点,侧重分析及计算能力的考查,把握原电池原理、电极反应为解答的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2.4g金属镁变成镁离子时失去的电子数为0.1NA | |
| B. | 标准状况下,11.2L CCl4所含的分子数为0.5NA | |
| C. | 0.5mol/L AlCl3溶液中Cl-的数目为1.5NA | |
| D. | 17g氨气中含有的电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
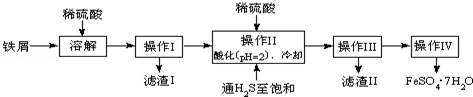
| 25℃时 | pH值 | 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 | FeS开始沉淀 | 3.0 |
| SnS沉淀完全 | 1.6 | FeS沉淀完全 | 5.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制240mL 0.1mol/LCuSO4溶液需称取胆矾6.3g | |
| B. | 金属氧化物一定是碱性氧化物 | |
| C. | 1L水中溶解58.5g NaCl,该溶液中NaCl的物质的量浓度为1 mol•L-1 | |
| D. | 胶体区别于其他分散系的本质特征是能够产生丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验设计 | 实验目的 |
| A | 过氧化钠与水反应 | 制备少量干燥的氧气 |
| B | 取铁在氧气中充分燃烧后的固体产物溶于稀硫酸,加KSCN溶液 | 检验铁的燃烧产物中含+3价铁 |
| C | 分别取大小相近的钠粒、钾粒投入水中,观察反应的剧烈程度 | 比较钠、钾的还原性强弱 |
| D | 将CO2气体通入Na2SiO3溶液中 | 比较C、Si元素非金属性的强弱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定是金属元素 | |
| B. | 一定能和氢氧化钠溶液反应生成氢气 | |
| C. | 一定是ⅡA族元素 | |
| D. | 可能是金属元素,也可能不是金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com