
【题目】下列关于硅酸盐产品的说法正确的是( )
A. 玻璃、水泥属于硅酸盐产品,陶瓷不属于硅酸盐产品
B. 普通玻璃的组成可表示为Na2SiO3·CaSiO3·4SiO2
C. 生产水泥的主要原料是纯碱、石灰石和石英
D. 生产玻璃的主要原料是黏土、石灰石
科目:高中化学 来源: 题型:
【题目】可以肯定溶液中存在大量SO42-的理由是
A. 加入AgNO3溶液,有白色沉淀产生
B. 加入稀盐酸溶液,无明显现象,再加入BaCl2溶液,产生白色沉淀
C. 加入Ba(OH)2溶液,产生白色沉淀,再加入稀盐酸,沉淀不溶解
D. 加入BaCl2溶液,产生白色沉淀,再加入稀盐酸,沉淀不溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验:
甲同学向1 mol·L1氯化铁溶液中加入少量的NaOH溶液;
乙同学直接加热饱和FeCl3溶液;
丙同学向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
(1)其中能得到Fe(OH)3胶体的同学是 。
(2)证明有Fe(OH)3胶体生成的实验操作是 。
(3)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带 电荷(填“正”或“负”)。
②向其中加入饱和Na2SO4溶液,产生的现象是 。
(4)Fe(OH)3胶体能稳定存在的主要原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的的是
A. 配制稀硫酸时,用10 mL量筒量取5.45 mL浓硫酸
B. 用稀硝酸清洗H2还原CuO后内壁附有Cu和Cu2O的试管
C. 将C与浓H2SO4反应产生的气体通入澄清石灰水检验CO2
D. 配制FeCl3溶液时,将FeCl3溶于热水中,冷却后加水稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO2+Ca(OH)2![]() CaCO3↓+H2O,CaCO3+CO2+H2O
CaCO3↓+H2O,CaCO3+CO2+H2O![]() Ca(HCO3)2,且Ca(HCO3)2易溶于水。试根据如图所示装置回答下列问题:
Ca(HCO3)2,且Ca(HCO3)2易溶于水。试根据如图所示装置回答下列问题:
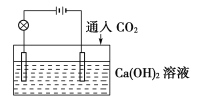
(1)通入CO2前,灯泡________(填“亮”或“不亮”)。
(2)开始通入CO2时,灯泡的亮度________。
(3)继续通入过量的CO2,灯泡的亮度________。
(4)下列四个图中,_______(填字母)能比较准确地反映出溶液的导电能力和通入CO2气体量的关系(x轴表示CO2通入的量,y轴表示导电能力)。
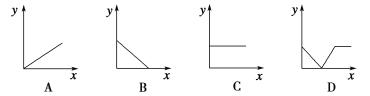
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 已知0.1molL-1的醋酸溶液中存在电离平衡:CH3COOHCH3COO-+H+,加少量烧碱溶液可使溶液中![]() 值增大
值增大
B. 饱和石灰水中加入少量CaO,恢复至原温后溶液的pH值不变
C. 25℃时,向水中加入少量固体CH3COONa ,水的电离平衡逆向移动,c(H+)降低
D. 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)<c(NO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学称取一定质量的MgCl2固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液(如下图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如下图乙所示。

请回答下列问题:
(1)溶解MgCl2固体所用的玻璃仪器有______(填字母)。
a.天平 b.烧杯
c.漏斗 d.玻璃棒
(2)OA段反应的离子方程式为______________________________________。
(3)AB段反应的离子方程式为______________________________________。
(4)在B点对应的溶液中滴加AgNO3溶液,观察到的现象是________,反应的离子方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】⑴反应N2(g)+3H2(g)2NH3(g)在恒温恒容条件下进行,下列情况中,处于平衡状态的是________;反应正向进行的是________;反应逆向进行的是_________.(填序号)
A.单位时间内消耗2mol N2,同时生成4mol NH3
B.单位时间内消耗3mol H2,同时生成2mol NH3
C.单位时间内生成2mol N2,同时生成6mol N—H键
D.混合气的密度不再随时间而改变
E.容器中气体的压强不再随时间而改变
F.单位时间内生成2mol NH3,同时又生成2mol H—H键
⑵恒温下,将amol N2与bmol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)2NH3(g)
反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,a =_________;
反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的体积分数为25%。平衡时NH3的物质的量为___________;
原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)=______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com