
. |
| M |
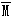 <28;
<28;


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
| A、1组 | B、2组 |
| C、3组 | D、不少于4组 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾的净水原理是因为明矾溶解于水水解生成带电的氢氧化铝胶体能够吸附水中的悬浮杂质 |
| B、CaO能与SO2反应,可作工业废气的脱硫剂 |
| C、从石油中可获得苯和甲苯等芳香烃 |
| D、人们可根据硫酸密度的大小来判断铅蓄电池是否需要充电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com