
| A. | 二氧化硫 | B. | 二氧化碳 | C. | 二氧化氮 | D. | 可吸入颗粒 |
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:选择题
| A. | (3m+n)mol | B. | ($\frac{5m}{2}$+$\frac{n}{2}$-3p)mol | C. | ($\frac{5m}{2}$+$\frac{n}{2}$)mol | D. | (3m+n+2p)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
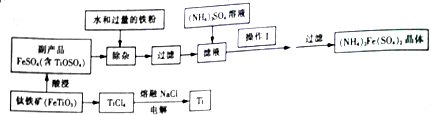
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正、逆反应速率都等于零 | B. | SO2、O2、SO3的浓度相等 | ||
| C. | SO2、O2、SO3在容器中共存 | D. | SO2、O2、SO3的浓度均不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)实验室可用如图装置制取乙炔图中A管的作用是调节水面的高度来控制反应的发生和停止,制取乙炔的化学反应方程式为CaC2+2H2O→C2H2↑+Ca(OH)2
(1)实验室可用如图装置制取乙炔图中A管的作用是调节水面的高度来控制反应的发生和停止,制取乙炔的化学反应方程式为CaC2+2H2O→C2H2↑+Ca(OH)2查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将AgNO3溶液滴入氨水中制银氨溶液 | |
| B. | 苯酚与苯甲醇(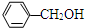 )分子组成相差一个-CH2原子团,因而它们互为同系物 )分子组成相差一个-CH2原子团,因而它们互为同系物 | |
| C. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| D. | 苯酚分子中由于羟基对苯环的影响,使苯环上的氢原子容易被取代 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com