
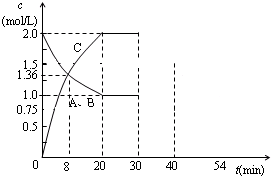
 Ⅰ、某容积不变的密闭容器中充入等物质的量的气体A和B,某温度下发生反应:
Ⅰ、某容积不变的密闭容器中充入等物质的量的气体A和B,某温度下发生反应:| △c |
| △t |
| △c |
| △t |
| 2.0mol/L |
| 20min |
| c2(c) |
| c(A)?c(B) |
| 2.0×2.0 |
| 1.0×1.0 |
 ,故答案:
,故答案: .
.

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
| A、C(CH3)3CH2OH |
| B、CH(CH3)2CHOHCH3 |
| C、CH3CH2CHOHCH3 |
| D、CH3CH2CHOHCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
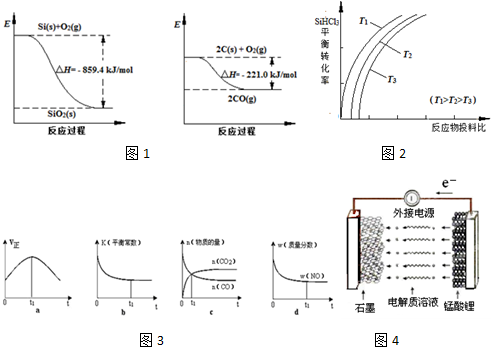
| 物质 | SiHCl3 | SiCl4 | AsCl3 |
| 沸点/℃ | 32.0 | 57.5 | 131.6 |
| 一定条件 |
| n(SiHCl3) |
| n(H2) |
| 催化剂 |
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
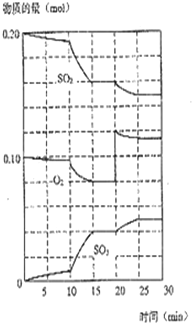 在一定条件下,二氧化硫和氧气发生如下反应:
在一定条件下,二氧化硫和氧气发生如下反应:| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学研究性学习小组设计制取氯气及探究其性质的方案,并按图所示装置完成实验.(A中发生反应的化学方程式为:MnO2+4HCl(浓)═MnCl2+Cl2↑+2H2O)
某化学研究性学习小组设计制取氯气及探究其性质的方案,并按图所示装置完成实验.(A中发生反应的化学方程式为:MnO2+4HCl(浓)═MnCl2+Cl2↑+2H2O)查看答案和解析>>
科目:高中化学 来源: 题型:
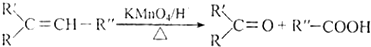
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、按系统命名法,有机物(CH3)2CHCH(CH2CH3)(CH2CH2CH3)的命名为:2-甲基-3-丙基戊烷 |
B、已知C-C键可以绕键轴自由旋转,结构简式为 ,分子中至少有7个碳原子处于同一直线上 ,分子中至少有7个碳原子处于同一直线上 |
C、 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O5Na4 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O5Na4 |
D、肌醇  与葡萄糖 与葡萄糖 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com