
化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求。某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好。[已知:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O]

(1)e处反应的离子方程式为________________________________________________。
该反应中发生反应的氧化剂和还原剂的物质的量之比为________。
(2)b处的实验现象为_____________________________________________,
d处的实验现象为_________________________________________________________。
(3)c处反应的化学方程式为___________________________ _____________________。
标准状况下,当有0.224 L Cl2被NaOH溶液吸收后,转移电子的物质的量为________mol。
(4)通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?________(填“能”或“不能”),若能,其氧化性由强到弱的顺序是________。
(1)2MnO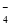 +16H++10Cl-===2Mn2++5Cl2↑+8H2O 1∶5
+16H++10Cl-===2Mn2++5Cl2↑+8H2O 1∶5
(2)溶液由无色变为蓝色 溶液由浅绿色变为红色
(3)Cl2+2NaOH===NaCl+NaClO+H2O 0.01
(4)能 KMnO4>Cl2>FeCl3
【解析】
试题分析:(1)浓盐酸易挥发,则挥发的HCl与高锰酸钾反应生成氯气,则e处的离子方程式为2MnO+16H++10Cl-===2Mn2++5Cl2↑+8H2O;该反应中的氧化剂是高锰酸钾,还原剂是氯化氢,所以氧化剂和还原剂的物质的量之比为2:10=1:5;
(2)e处产生的氯气与KI反应生成碘单质,碘与淀粉变蓝色,所以b处的溶液由由无色变为蓝色;d处的氯化亚铁与氯气反应生成氯化铁,铁离子与KSCN溶液反应溶液变红色,所以d处溶液由浅绿色变为红色;
(3)c处的氢氧化钠溶液与氯气反应生成氯化钠、次氯酸钠、水,化学方程式为Cl2+2NaOH===NaCl+NaClO+H2O;标准状况下, 0.224 L Cl2的物质的量是0.01mol,氯气在该反应中既作氧化剂又作还原剂,所以转移电子的物质的量是0.01mol;
(4)根据e、d处的实验现象结合氧化还原反应规律可知,高锰酸钾的氧化性大于氯气,氯气的氧化性大于氯化铁,所以可以比较三者的氧化性的强弱,顺序是KMnO4>Cl2>FeCl3
考点:考查氧化还原反应的分析,实验现象的判断,物质氧化性的比较


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015届江西省上学期高三第一次月考化学试卷(解析版) 题型:选择题
下列离子或分子组中能大量共存,且满足相应要求的是 ( )
选项 | 离子或分子 | 要求 |
A | K+、NO | c(K+)<c(Cl-) |
B | Fe3+、NO | 滴加盐酸立即有气体产生 |
C | NH | 滴加NaOH溶液立即有气体产生 |
D | Na+、HCO | 滴加氨水立即有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源:2015届江西省新余市高三第二次模拟考试化学试卷(解析版) 题型:选择题
短周期元素R、T、Q、W、G在元素周期表中的相对位置如下图所示,其中R与T原子序数之和为20,下列判断正确的是
|
| R |
| |
T | Q |
| W | G |
A.离子半径:T> W
B.最高价氧化物对应水化物的酸性:Q >W>G
C.最简单气态氢化物的热稳定性:Q < R
D.T和G组成的化合物甲溶于水,其水溶液呈中性
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
阿伏加德罗常数的值为6.02×1023mol-1,下列叙述中错误的是:
①12.4g 白磷晶体中含有的P-P键数是0.6×6.02×1023
②含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0. 1×6.02×1023
③7.8g Na2S和Na2O2的混合物中含有的阴离子数大于0.1×6.02×1023
④2mol SO2和1mol O2在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数等于2×6.02×1023
⑤2.9g 2CaSO4?H2O含有的结晶水分子数为0.02×6.02×1023
A.①②③④⑤ B. ①③④⑤ C. ②③④⑤ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
可用于电动汽车的铝?空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是 ( )。
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为O2+2H2O+4e-
===4OH-
B.以NaOH溶液为电解液时,负极反应为Al+3OH--3e-===Al (OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
用下列实验装置进行相应实验,能达到实验目的的是

A.用图2 所示装置除去Cl2中含有的少量HCl
B.用图3 所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图4 所示装置制取少量纯净的CO2气体
D.用图5 所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三第一次模拟考试化学试卷(解析版) 题型:选择题
下列有关判断、叙述正确的是( )
A.质量分数为W的氨水其浓度为C1 mol/L,则质量分数为2W的氨水,其浓度大于2C1 mol/L
B.3.2克的甲烷与标准状况下8.96 L的水所含有的氢原子数相同
C.铅蓄电池中放电时转移2NA个电子,则电池内消耗4 mol H2SO4
D.等质量的SO2与SO3所含有的氧原子数之比为5:6
查看答案和解析>>
科目:高中化学 来源:[同步]2015年课时练(鲁科版必修2)课时16苯的结构和性质(解析版) 题型:选择题
下列变化属于化学变化的是( )
A.石油分馏
B.用四氯化碳从溴水中萃取溴
C.煤的干馏
D.苯散发出特殊气味
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com