
����Ŀ���̶��ݻ�Ϊ2 L���ܱ������з�����ӦxA(g)+yB(g) ![]() zC(g)��ͼI��ʾ200��ʱ�����и����ʵ�����ʱ��ı仯��ϵ��ͼII��ʾƽ��ʱƽ�ⳣ��K���¶ȱ仯�Ĺ�ϵ�����ͼ���жϣ����н�����ȷ����
zC(g)��ͼI��ʾ200��ʱ�����и����ʵ�����ʱ��ı仯��ϵ��ͼII��ʾƽ��ʱƽ�ⳣ��K���¶ȱ仯�Ĺ�ϵ�����ͼ���жϣ����н�����ȷ����
![]()
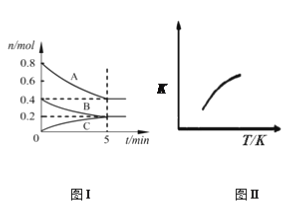
A. 200��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ����Ӧ����v(A)��0.08mol��L-1��min-1
B. ��0~5 minʱ�����������Ƚ�������Ϊm kJ����÷�Ӧ���Ȼ�ѧ����ʽ�ɱ�ʾΪ��2A + B ![]() C ��H = +5m kJ/mol
C ��H = +5m kJ/mol
C. 200��ʱ�����ڵ�6 min������ϵ�м���1molAr��A��ת���ʲ���
D. 200��ʱ��ƽ����ٳ���2 mol B��2 mol Cʱ��v����v��
���𰸡�C
��������
A�����ݻ�ѧ��Ӧ���ʵ���ѧ����ʽ��v(A)=(0.8��0.4)/(5��2)mol/(L��min)=0.04 mol/(L��min)����A����B����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȵ������ʵ����仯֮�ȣ�x:y:z=(0.8��0.4):(0.4��0.2):0.2=2:1:1����Ӧ����ʽΪ2A(g)+ B(g) ![]() C(g)���¶����ߣ���ѧƽ�ⳣ�������˷�Ӧ����Ӧ�����ȷ�Ӧ���Ȼ�ѧ��Ӧ����ʽΪ2A(g)+ B(g)
C(g)���¶����ߣ���ѧƽ�ⳣ�������˷�Ӧ����Ӧ�����ȷ�Ӧ���Ȼ�ѧ��Ӧ����ʽΪ2A(g)+ B(g) ![]() C(g) ��H=��5mkJ��mol��1��Cѡ���Ȼ�ѧ��Ӧ����ʽû�б������ʵ�״̬����B����C������״̬�£�����Ƿ�Ӧ���壬���Ũ�Ȳ��䣬��A��ת���ʲ��䣬��C��ȷ��D�� 200��ʱ���ﵽƽ�⣬ƽ�ⳣ��K=
C(g) ��H=��5mkJ��mol��1��Cѡ���Ȼ�ѧ��Ӧ����ʽû�б������ʵ�״̬����B����C������״̬�£�����Ƿ�Ӧ���壬���Ũ�Ȳ��䣬��A��ת���ʲ��䣬��C��ȷ��D�� 200��ʱ���ﵽƽ�⣬ƽ�ⳣ��K=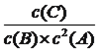 ��������ֵ�����K=25��ƽ����ٳ���2molB��2molC����ʱQc=25=K����ѧƽ�ⲻ�ƶ�����v��=v�棬��D����
��������ֵ�����K=25��ƽ����ٳ���2molB��2molC����ʱQc=25=K����ѧƽ�ⲻ�ƶ�����v��=v�棬��D����


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ʻ���COS������ΪѬ���������ӽṹ�루CO2�����ơ��ش��������⣺
(1) ̼ԭ�ӵĺ�������Ų�ʽΪ____������ʻ����Ԫ���У��뾶����ԭ���������____�ֲ�ͬ�����ĵ��ӡ�
(2)�ʻ���Ϊ____(����ԡ��Ǽ��ԡ�)���ӣ��ʻ���ĵ���ʽΪ____��
(3)�����ȶ��� CO2 ���� CS2 ��ԭ��____________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��һ�ֳ���������F��һ�ֺ��ɫ�������Ը���ͼ��ת����ϵ���ش��������⡣
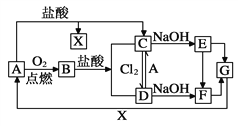
��1��д��A��C��F��G�Ļ�ѧʽ:A________��C_________��F_________��G_________��
��2������D�������ӵķ���_____________________________________________��
��3������C��ҺʱΪʲôҪ�ӹ���A_____________________________________��
��4��д������ת�������ӷ���ʽC��D��____________________________________����Eת��ΪF�������� _________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ж���ȷ����

A. ͼ�٣���CH4��Cl2�����Ϊ1:2��ά���㹻����Ӧʱ�䣬CH4��ȫ�����CCl4
B. ͼ�ڣ����Ƭ������������ʵ���е����Ƭ���ò�ͬ
C. ͼ�ۣ�������ϩ����Ȳ���ĵ�һ���ʼ�ͬ�����ﺬ̼����Cԭ�����ı仯���߷ֱ�Ϊa��b��c
D. ͼ�ܣ���a������������PH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2.0 mol PCl3��1.0 mol Cl2�������������ܱ������У���һ�������·���������Ӧ��PCl3(g)��Cl2(g)![]() PCl5(g)����ƽ��ʱ��PCl5Ϊ0.40 mol�������ʱ����1.0 mol PCl3��0.50 mol Cl2������ͬ�¶����ٴ�ƽ��ʱ������˵������ȷ����
PCl5(g)����ƽ��ʱ��PCl5Ϊ0.40 mol�������ʱ����1.0 mol PCl3��0.50 mol Cl2������ͬ�¶����ٴ�ƽ��ʱ������˵������ȷ����
A. PCl5�����ʵ�������0.20 molB. PCl5��������������
C. ƽ�ⳣ������D. �������Ļ���ɫ��dz
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ1��ͭпԭ���ʾ��ͼ��ͼ2�У�x���ʾʵ��ʱ���������ĵ��ӵ����ʵ�����y���ʾ��������
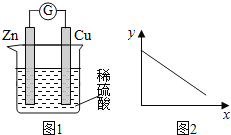
A. ͭ�������� B. c(Zn2��) C. c(H��) D. c(SO42-) -
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E���ֶ���������Ԫ�أ�ԭ��������A��E������AԪ�������������Ǵ�����������2������B�������Ӻ�C������������ԭ�ӵĵ��Ӳ�ṹ��ͬ������ͨ��״���£�B�ĵ��������壬0.1 mol B��������������������ȫ��Ӧ����0.4 mol����ת�ơ���C�ĵ����ڵ�ȼʱ��B�ĵ��ʳ�ַ�Ӧ�����ɵ���ɫ�Ĺ��壬�˵���ɫ��������AB2��Ӧ������B�ĵ��ʡ���D����̬�⻯��������ۺ�������ܷ���������ԭ��Ӧ����ش��������⣺
��1��д��AԪ�ص����������ĵ���ʽ_____________��
��2��BԪ�������ڱ��е�λ��Ϊ_____________�� ����
��3��B������C�����ڵ�ȼʱ��Ӧ����������������ѧ��������______________��
��4��DԪ�صĵͼ���������E�ĵ��ʵ�ˮ��Һ��Ӧ�Ļ�ѧ����ʽΪ______________��
��5��C��D���γ�2��1�Ļ�����õ���ʽ��ʾ�û�������γɹ���______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п�̵�صķ�Ӧ����ʽΪ 2MnO2��Zn��2H2O===2MnOOH��Zn(OH)2���乹����ͼ��ʾ���й�˵������ȷ����(����)

A.������Ӧʽ��Zn��2OH����2e��===Zn(OH)2
B.�ŵ�ʱ����MnO2�õ����ӣ�����������Ӧ
C.�õ��ʹ��һ��ʱ����ҺpH����
D.�ŵ�ʱ��п��ʧȥ�ĵ��ӣ��Ӹ���ͨ�����·��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������и����������ʣ�
A��O2��O3
B.![]() ��
��![]()
C��CH3CH2CH2CH3��CH3CH2CH(CH3)CH3
D��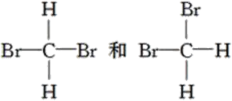
E��CH3CH2CH2CH3��![]()
(1)________����������Ϊͬλ�ء�
(2)________���������ʻ�Ϊͬ�������塣
(3)________��������������ͬϵ�
(4)________�������ʻ�Ϊͬ���칹�塣
(5)________����������ͬһ���ʡ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com