
【题目】如图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。

(1)写出甲池中负极电极反应式_________________________________________
(2)写出A电极的电极反应式____________________________________________
(3)写出丙中反应的离子方程式___________________________________________
(4)工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。则乙中A极析出的气体在标准状况下的体积为_____________________。
【答案】![]()
![]()
![]()
![]()
【解析】
(1)甲醇燃料电池是原电池反应,甲醇在负极失电子发生氧化反应,电极反应为:![]() ,故答案为:
,故答案为:![]()
(2)100mL1mol/L的硫酸铜溶液中含有铜离子0.1mol,硫酸根离子0.1mol,当电解硫酸铜溶液时,阳极反应式为:![]() ,故答案为:
,故答案为:![]() ;
;
(3)丙中反应的离子方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(4)工作一段时间后,断开K,此时A、B两极上产生的气体体积相同,分析电极反应,B为阴极,溶液中铜离子析出,氢离子得到电子生成氢气,设生成气体物质的量为X,溶液中铜离子物质的量为![]() ,电极反应为:
,电极反应为:
Cu2++2e-=Cu,2H++2e-=H2↑;
0.1mol 0.2mol 2x x
A电极为阳极,溶液中的氢氧根离子失电子生成氧气,电极反应为:
4OH--4e-=2H2O+O2↑;
4x x
得到0.2+2x=4x
x=0.1mol
乙中A极析出的气体是氧气物质的量为![]() ,在标准状况下的体积为
,在标准状况下的体积为![]() 故答案为:
故答案为:![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】探索CO2与CH4的反应使其转化为CO和H2,对减缓燃料危机,减少温室效应具有重要意义。回答下列问题
(1)已知:①CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.1kJ·mol-1
CO(g)+3H2(g) △H1=+206.1kJ·mol-1
②2H2(g)+CO(g)![]() CH3OH(1) △H2=-128.3kJ·mol-1
CH3OH(1) △H2=-128.3kJ·mol-1
③2H2(g)+O2(g)![]() 2H2O(g) △H3=-483.6kJ·mol-1
2H2O(g) △H3=-483.6kJ·mol-1
25℃时,在合适的催化剂作用下,采用甲烷和氧气一步合成液态甲醇的热化学方程式为______________________。
(2)向某密闭恒容容器中通入物质的量浓度均为0.1mol·L-1的CH4与CO2,在一定条件下发生反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如图所示。
2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如图所示。
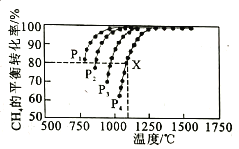
①工业生产时一般会选择在P4和1250℃条件下进行反应,请解释其原因______________________。
②在压强为P4、1100℃的条件下,该反应在5min时达到平衡点X,则0-5min内,用CO表示该反应平均速率为___________;该温度下,反应的平衡常数为___________(保留3位有效数字)。
(3)工业上用CO和H2制取甲醇反应方程式为2H2(g)+CO(g)![]() CH3OH(g)。对于该合成反应,若通入的CO的物质的量一定,如图为4种投料比[n(CO)︰n(H2)分别为5︰7、10︰17、5︰9、1︰2]时,反应温度对CO平衡转化率的影响曲线。
CH3OH(g)。对于该合成反应,若通入的CO的物质的量一定,如图为4种投料比[n(CO)︰n(H2)分别为5︰7、10︰17、5︰9、1︰2]时,反应温度对CO平衡转化率的影响曲线。
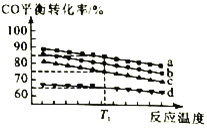
①曲线b对应的投料比是___________
②当反应在曲线a、b、c对应的投料比下达到相同的平衡转化率时,对应的反应温度和投料比的关系是___________。
③投料比为10︰17反应温度为T1时,平衡混合气体中CO的物质的量分数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】成熟的苹果中含有淀粉、葡萄糖和无机盐等,某课外兴趣小组设计了一组实验证明某些成分的存在,请你参与并协助他们完成相关实验。
(1)用小试管取少量的苹果汁,加入_______(填名称),溶液变蓝,则证明苹果中含有淀粉。
(2)利用含淀粉的物质可以生产醋酸。下面是生产醋酸的流程图,试回答下列问题:
![]()
B是日常生活中有特殊香味的常见有机物,在有些饮料中含有B。
①写出化学方程式,并注明反应类型。
B与醋酸反应:____________________________,属于______________反应。
B→C____________________________,属于____________________________反应。
②可用于检验A的试剂是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:

(1)B极是电源的__________,一段时间后,甲中溶液颜色_________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明_______________,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为_______。
(3)现用丙装置给铜件镀银,则H应该是_______(填“镀层金属”或“镀件”),电镀液是________溶液。当乙中溶液的C(OH-)=0.1mol/L时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为________,甲中溶液的pH_________(填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,转化过程表示如图。下列说法正确的是 ( )
![]()
A.x﹥yB.SO2是该反应的催化剂
C.MFe2Ox是还原剂D.SO2发生了分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是
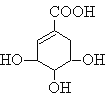
A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示AlCl3溶液与NaOH溶液滴加过程中微粒数量的关系曲线。 判断下列说法不正确的是( )

A.A线表示Al3+的物质的量的变化
B.x表示NaOH的物质的量
C.C线表示Al(OH)3的物质的量的变化
D.D线表示Al(OH)3的物质的量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.使酚酞变红色的溶液中:Na+、Al3+、![]() 、Cl-
、Cl-
B.与Al反应能放出H2的溶液中:Fe2+、K+、![]() 、
、![]()
C.![]() =1×10-13mol/L的溶液中:
=1×10-13mol/L的溶液中:![]() 、Ca2+、Cl-、
、Ca2+、Cl-、![]()
D.水电离的c(H+)=1×10-13mol/L的溶液中:K+、Na+、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是![]()
A.白磷![]() 为正四面体结构,则
为正四面体结构,则![]() 与
与![]() 所含共价键数目之比为3:1
所含共价键数目之比为3:1
B.1mol乙酸与足量的![]() 充分发生酯化反应可生成
充分发生酯化反应可生成![]() 分子
分子![]() 个
个
C.![]() 与
与![]() 的混合物中所含中子数为
的混合物中所含中子数为![]()
D.浓度均为![]() 的醋酸和醋酸钠溶液等体积混合,溶液中
的醋酸和醋酸钠溶液等体积混合,溶液中![]() 和
和![]() 的总数为
的总数为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com