
����ѧ��ѡ��3�����ʽṹ�����ʡ���15�֣���֪λ��Ԫ�����ڱ�ǰ�����ڵ�����Ԫ��A��B��C��D��E��F��ԭ������֮��Ϊ107�������ǵĺ˵������������Bԭ�ӵ�p�������������⻯��е���ͬ��Ԫ������͵ģ�Dԭ�ӵõ�һ�����Ӻ�3p���ȫ������A��C���γ�A2C�����ӻ�������е��������������һ�����Ӳ㣬E4�����Ӻ��ԭ�ӵĺ�������Ų���ͬ����ش��������⣺
��1��A��B��C��D�ĵ�һ��������С�����˳����____________����Ԫ�ط��ţ�
��2��������BD3�ķ��ӿռ乹�Ϳ�����Ϊ_________��B��ԭ�ӹ���ӻ�����Ϊ_______��
��3����֪FԪ���������ں���ƫ��ʱ����Ӱ��O2�����ڵ��������䡣��֪F2����KCN��Һ��Ӧ��F��CN��2���������������KCN��Һʱ�����ܽ⣬����������F�Ļ�̬ԭ�Ӽ۵����Ų�ʽΪ________________��CN����___________��һ�ַ��ӣ���Ϊ�ȵ����壬��1��CN���Цм���ĿΪ___________��
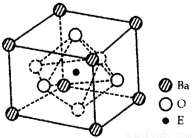
��4��EO2��̼�ᱵ������״̬�·�Ӧ�����þ���ľ����ṹ��ͼ��ʾ����÷�Ӧ�Ļ�ѧ����ʽΪ__________
�ڸþ����У�E4��������Ϊ��Ϊ___________�����þ����߳�Ϊa nm�ɼ���þ�����ܶ�Ϊ__________g��cm3�������ӵ�����ΪNA��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�����и�������������Կ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�FeBr2��Һ�������������
A���μ�KI-������Һ��Ϊ��ɫ
B������Һ��Cu2+��NH4+��SO42����Cl�� ���Դ�������
C���������ữ��AgNO3��Һ��Ӧ�г������ɲ��ų�����
D�������Һ��ͨ�����Cl2����Ӧ�����ӷ���ʽ��2Fe2+��4Br����3Cl2==2Fe3+��2Br2��6Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ���������������ѧ���������п��ԣ���ģ����ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ����ʹ����ȷ��
A����ԭ��������ߵĵ��ӵĵ�����ͼ��
B��35Cl�� 37Cl��Ϊͬ��������
C��CH4���ӵı���ģ�ͣ�
D��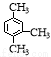 ��������1,3,4-���ױ�
��������1,3,4-���ױ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�������и�����ѧ�ڵ������ʼ쿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
����ѧ��ѡ��2����ѧ�뼼������15�֣����Ṥҵ�ķ������������õĹ����������£�
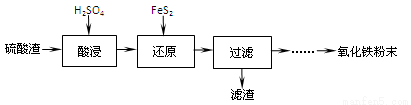
ע������������Ҫ��Fe2O3��SiO2��Al2O3��MgO�����ʣ�
��1���������������Ҫ�ʵ�������Ŀ���ǣ���������Ľ����ʣ��� ��
��2������ԭ���ǽ�Fe3��ת��ΪFe2����ͬʱFeS2������ΪSO42�����÷�Ӧ�����ӷ���ʽΪ ��
��3��Ϊ�ⶨ��������������Һ��Fe3�������Կ��Ƽ���FeS2������ʵ�鲽��Ϊ��
ȷ��ȡһ���������������Һ����ƿ�У�����HCl���Թ���SnCl2���ټ�HgCl2��ȥ������SnCl2���Զ�����������Ϊָʾ������K2Cr2O7����Һ�ζ����йط�Ӧ����ʽ���£�
2Fe3����Sn2����6Cl����2Fe2����SnCl62����
Sn2����4Cl����2HgCl2��SnCl62����Hg2Cl2����
6Fe2����Cr2O72����14H����6Fe3����2Cr3����7H2O��
����SnCl2����������ⶨ��Fe3���� ���ƫ�ߡ�����ƫ�͡��������䡱����ͬ����
��������HgCl2����ⶨ��Fe3���� ��
��4���ٿ�ѡ�� �����Լ���������Һ�к���Fe3+�����������Fe2+�ɱ�������O2�����������ӷ�Ӧ����ʽ��ʾ�� ��
����֪����������������������ʽ����ʱ��Һ��pH���±���
������ | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
��ʼ���� | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
��ȫ���� | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
ʵ���ѡ�õ��Լ��У�ϡHNO3��Ba(NO3)2��Һ������KMnO4��Һ��NaOH��Һ��Ҫ���Ʊ������в������ж����塣������ɡ����ˡ������Һģ���Ʊ���������ʵ�鲽�裺
��һ���������� ������д���������
�ڶ��������� ������д���������
�����������룬ϴ�ӣ�
���IJ�����ɣ���ĥ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�������и�����ѧ�ڵ������ʼ쿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ijѧ������˿��Cl2Ϊԭ�Ͻ�����������ʵ�顣
�ӷ���Ƕ����з�����ȷ����
A��ʵ��١��۷�Ӧ�Ƶõ����ʾ�Ϊ������
B��ʵ��ڡ��۾�δ����������ԭ��Ӧ
C��ʵ��ڡ��۾�Ϊ���ȷ�Ӧ
D��ʵ��١������漰�����ʾ�Ϊ����ʻ�ǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и���������⣨�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ�飬��ѡװ����ȷ����
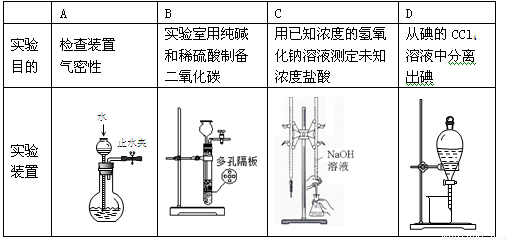
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и���ѧҵˮƽģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ������
����Ϊ����ѧ��Ӧԭ����ѡ��4����ģ��ѡ���⣬ÿ��2�֣���20�֡�
��1��������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϡ�
������ȼ����ֵ�ߡ�ʵ���ã��ڳ��³�ѹ�£�1 mol H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ���������ʾH2ȼ���ȵ��Ȼ�ѧ����ʽ�ǣ� ��
A.H2(g) +1/2 O2(g)=H2O(g) ��H =+285.8 kJ/mol
B.H2(g) +1/2 O2(g)=H2O(l) ��H =��285.8 kJ/mol
C.H2(g) +1/2 O2(g)=H2O(l) ��H =+285.8 kJ/mol
D.H2 +1/2 O2 =H2O ��H =��285.8 kJ/mol
������ȼ�ϵ������ת���ʸߣ����й����ķ�չǰ��������ȼ�ϵ���У�������ԭ��Ӧ�������� ���������������������
�������Ǻϳɰ�����Ҫԭ�ϣ��ϳɰ���Ӧ���Ȼ�ѧ����ʽ���£�
N2(g)��3H2(g) 2NH3(g) ��H����92.4 kJ/mol
2NH3(g) ��H����92.4 kJ/mol
��Ӧ�ﵽƽ��������¶���Ӧ���� �������С������ƽ�⽫�� �������Ӧ�����淴Ӧ�����ƶ���
��2��п�����������ѹƽ�ȣ��㷺���ڵ����ֱ�����������������������͵����������������Һ��KOH��Һ������ܷ�ӦΪZn��Ag2O=ZnO��2Ag����ش��������⣺
�ٸõ�صĸ��������� ����ع���ʱ���������� (�������������)�ƶ���
�ڵ缫����п������п���ڿ��������ճ�����п��Ȼ����̼��ԭ����п����ȡ���÷�Ӧ�Ļ�ѧ����ʽΪZnO��C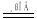 Zn��CO�����˷��� ����ѡ����ĸ���ţ���
Zn��CO�����˷��� ����ѡ����ĸ���ţ���
A����ⷨ B���Ȼ�ԭ�� C���ȷֽⷨ
��3�����г�����������Һ��(A)0.1mol/L��NaCl��Һ (B)0.1mol/LNH4Cl��Һ
����Һ(A)��pH 7�����������������=������
����Һ(B)�� �ԣ���ᡱ��������С����������¶ȿ��� ����ٽ��������ơ���NH4Cl��ˮ�⡣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и���ѧҵˮƽģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
235 92U��һ����Ҫ�ĺ�ȼ�ϣ����С�92����ָ��ԭ�ӵ�
A�������� B�������� C�������� D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫�߿���ɽ�и�����ģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶��£���һ�����0��1mol/LHCl��Һ����μ����Ũ�ȵİ�ˮ��Һ����Һ��pOH[pOH=-lgc(OH-��]��pH�ı仯��ϵ��ͼ��ʾ��������˵���������
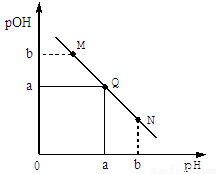
A��Q�����İ�ˮ��Һ���������HCl��Һ�����
B��M����ʾ��Һ������������Q��
C��M���N����ʾ��Һ��ˮ�ĵ���̶���ͬ
D��N����ʾ��Һ��c(NH4+�� �� c(OH����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com