
【题目】下图中的每一个方格表示有关的一种反应物或生成物,其中X为正盐,A、C、D均为无色气体,且气体C的水溶液显碱性。

(1)用化学用语按要求填空
X的化学式为:____,X中含有化学键类型为_______;A的电子式:____;G的化学式为_________。
(2)写出反应①的化学方程式________________。
(3)写出反应②的离子方程式________________。
(4)过量的Fe粉与G的稀溶液反应,向反应后溶液中加入碱溶液,现象是_________,反应的离子方程式为
_________________________;________________。
【答案】 (NH4)2CO3 离子键、共价键 ![]() HNO3 2N2O2 + 2H2O ==4NaOH + O2↑ Cu +4H+ +2NO3-=Cu2+ +2NO2↑+ 2H2O 先产生白色沉淀,随后变为灰绿色,最后生成红褐色沉淀 Fe2+ + 2OH_ ===Fe(OH)2 4Fe(OH)2 + O2 + 2H2O===4Fe(OH)3
HNO3 2N2O2 + 2H2O ==4NaOH + O2↑ Cu +4H+ +2NO3-=Cu2+ +2NO2↑+ 2H2O 先产生白色沉淀,随后变为灰绿色,最后生成红褐色沉淀 Fe2+ + 2OH_ ===Fe(OH)2 4Fe(OH)2 + O2 + 2H2O===4Fe(OH)3
【解析】X为正盐,A、C、D均为无色气体,且气体C的水溶液显碱性,C是氨气;X既能与盐酸反应,又能与NaOH反应,都生成气体,应为弱酸铵盐,气体A能与过氧化钠反应,A为CO2,则X应为碳酸铵,B为H2O,结合转化关系可知,D为O2,E为NO2,G为HNO3,则
(1)根据以上分析可知X的化学式为(NH4)2CO3,其中含有化学键类型为离子键和共价键;CO2的电子式为![]() ;G的化学式为HNO3。(2)反应①为二氧化碳和过氧化钠的反应,反应方程式为2N2O2 + 2H2O=4NaOH + O2↑。(3)反应②是铜和浓硝酸反应生成硝酸铜、二氧化氮和水,离子方程式为 Cu +4H+ +2NO3-=Cu2+ +2NO2↑+ 2H2O。(4)过量的Fe粉与G的稀溶液反应生成硝酸亚铁,因此向反应后溶液中加入碱溶液,现象是先产生白色沉淀,随后变为灰绿色,最后生成红褐色沉淀,反应的离子方程式为Fe2+ + 2OH-=Fe(OH)2↓、4Fe(OH)2 + O2 + 2H2O=4Fe(OH)3。
;G的化学式为HNO3。(2)反应①为二氧化碳和过氧化钠的反应,反应方程式为2N2O2 + 2H2O=4NaOH + O2↑。(3)反应②是铜和浓硝酸反应生成硝酸铜、二氧化氮和水,离子方程式为 Cu +4H+ +2NO3-=Cu2+ +2NO2↑+ 2H2O。(4)过量的Fe粉与G的稀溶液反应生成硝酸亚铁,因此向反应后溶液中加入碱溶液,现象是先产生白色沉淀,随后变为灰绿色,最后生成红褐色沉淀,反应的离子方程式为Fe2+ + 2OH-=Fe(OH)2↓、4Fe(OH)2 + O2 + 2H2O=4Fe(OH)3。


科目:高中化学 来源: 题型:
【题目】糖类、脂肪和蛋白质是维持人体生命活动中所必须的三大营养物质。下列说法正确的是
A.植物油是纯净物 B.淀粉遇碘水变蓝色
C.葡萄糖能发生水解反应 D.蛋白质水解的最终产物是葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示,下列说法正确的是( )
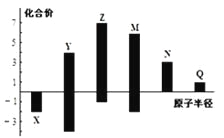
A. 金属性:N>Q
B. 最高价氧化物对应水化物酸性:M>Y>N
C. 简单离子半径:Q>N>X
D. 原子序数:Z>M>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述中正确的是
4NO(g)+6H2O(g),下列叙述中正确的是
A.化学反应速率的关系是2v逆(NH3)=3v正(H2O)
B.若单位时间内生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态
C.达到化学平衡时,若增大容器的体积,则正反应速率减小,逆反应速率增大
D.达到化学平衡时4v正(O2)=5v逆(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。下列有关评价正确的是

A.根据图Ⅰ所示实验,可以根据澄清石灰水是否变浑浊鉴别碳酸钠和碳酸氢钠固体
B.在图Ⅱ所示实验的左右两只试管中加入足量的盐酸,然后向两个气球中分别加入等物质的量的碳酸钠和碳酸氢钠固体,根据反应后气球的大小可鉴别两种固体
C.与实验Ⅲ相比,实验Ⅳ的突出优点是可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
D.若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则小试管B中装入的固体是碳酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应过程或实验现象的叙述中,正确的是( )
A. 氯气的水溶液可以导电,说明氯气是电解质
B. 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的
C. 氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气
D. 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,说明BaCl2溶液具有酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应:H2(g) + CO2(g)![]() H2O(g)+CO(g)的平衡常数K =9/4该温度下,在甲、乙两个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
H2O(g)+CO(g)的平衡常数K =9/4该温度下,在甲、乙两个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
起始浓度 | 甲 | 乙 |
c(H2)/mol L-1 | 0.010 | 0.020 |
C(CO2)/mol·L-1 | 0.010 | 0.010 |
下列判断正确的是
A. 平衡时,甲容器中H2的转化率为60%
B. 平衡时,乙容器中H2的转化率大于60%
C. 平衡时,乙容器中c(H2)是甲容器中的2倍
D. 反应开始时,甲容器中的反应速率比乙容器中的反应速率快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂中主要含SiO2、ZnO、CuS及少量的Fe3O4。某同学以该废催化剂为原料制备皓矾(ZnSO4·7H2O)和蓝矾(CuSO4·5H2O)的实验流程如图所示。

已知:CuS不溶于稀硫酸。
(1)滤渣1的主要成分为________(填化学式)。
(2)实验室用浓H2SO4配制250mL0.50mol/L硫酸溶液时,不需要用到的仪器是________ (填字母)。
A.玻璃棒 B.胶头滴管 C.漏斗 D.容量瓶 e.天平 f.烧杯
(3)现有KMnO4溶液、NaOH溶液、碘水等试剂。用所提供的试剂检验滤液1中是否含有Fe2+的方法为______________。
(4)向盛有滤渣1的反应器中加入硫酸和H2O2溶液时发生反应的化学方程式为____________.(已知滤渣2中含有S)
(5)某同学称取m1废催化剂进行实验,其中CuS的质量分数为x,实验完成之后,得到m2gCuSO4·5H2O,则铜元素的回收率为________________。(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体的组成可用H2C2O4·xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100mL水溶液。量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L-1的KMnO4溶液滴定,所发生的反应为:KMnO4+H2C2O4+H2SO4 -K2SO4+CO2↑+MnSO4+H2O(未配平)
试回答:
(1)实验中,KMnO4溶液应装在___________式滴定管中。
(2)滴定过程中需要加入的指示剂为___________(填指示剂的名称或“不需要”),确定反应达到滴定终点时的现象是 。
(3)图I表示100mL量筒中液面的位置,A与B,B与C,刻度间均相差10mL,如果刻度A为30,量筒中液体的体积是________mL。图II表示25mL滴定管中液面的位置,D与E刻度间也相差10mL,如果D处的读数是5,则滴定管中液体的读数是________mL。

(4)以下操作造成测定结果偏高的原因可能是 。(用符号填写)
A.滴定前滴定管有气泡,滴定后气泡消失
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管
(5)在滴定过程中若用a mol·L-1的KMnO4溶液V mL,则所配制的草酸溶液的物质的量浓度为____________mol·L-1,由此可计算x的值是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com