
鲜榨苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色 Fe3+。若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生。这说明维生素C具有
A.氧化性 B.还原性 C.酸性 D.碱性
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届湖北省高三上学期期中考试化学试卷(解析版) 题型:选择题
全钒液流电池是一种新型的绿色环保储能电池,该电池性能优良,其电池总反应为:v3++VO2++H2O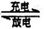 VO2++2H++V2+。下列叙述正确的是
VO2++2H++V2+。下列叙述正确的是
A.充电时阳极附近溶液的酸性减弱
B.充电时阳极反应式为:VO2++2H++e-=VO2++H2O
C.放电过程中电解质溶液中阳离子移向负极
D.放电时每转移1mol电子,负极有1mol V2+被氧化
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上第二次模拟化学试卷(解析版) 题型:选择题
已知Fe2+结合S2-的能力大于结合OH-的能力,而Al3+则正好相反。在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是
A.Al2S3、FeS和S B.Fe(OH)3和Al(OH)3
C.Fe2S3和 Al(OH)3 D.FeS、Al(OH)3和S
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
一定条件下反应2AB(g)  A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A.单位时间内生成n molA2,同时消耗2n molAB
B.容器内三种气体AB、A2、B2共存
C.容器中各组分的体积分数不随时间变化
D.AB的消耗速率等于A2的消耗速率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州市高一上学期期中测试化学试卷(解析版) 题型:选择题
将少量氯水加入KI溶液中,振荡,再加入CCl4,振荡,静置,观察到的现象是( )
A.有紫黑色固体析出 B.形成均匀的紫红色溶液
C.液体分层,下层紫红色 D.液体分层,上层紫红色
查看答案和解析>>
科目:高中化学 来源:2016届浙江省深化课程改革协作校高三上学期11月期中联考化学试卷(解析版) 题型:选择题
生活中遇到的某些问题,常常涉及到化学知识,下列叙述正确的是
A.废旧电池必须进行集中处理的主要原因是回收其中的碳电极
B.钠、镁等金属着火,可用CO2灭火
C.“雨后彩虹”和“海市蜃楼”现象的出现与胶体的性质有关
D.“加碘食盐”“含氟牙膏”“富硒营养品”“高钙牛奶”“加铁酱油”等等,这里的碘、氟、硒指的是分子,钙、铁则分别是钙离子和铁离子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列物质中含分子数最多的是
A.标准状况下44.8L氨气
B. 66gCO2
C.标准状况下90mL水
D. 3.01×1023个氢分子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷(解析版) 题型:填空题
硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个有一个奇迹。
(1)新型陶瓷Si3N4的熔点高、硬度大、化学性质稳定。工业上可以采用化学气相沉积法,在H2的保护下,使SiCl4与N2反应生成Si3N4沉积在石墨表面,写出该反应的化学方程式 。
(2)一种用工业硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1420℃,高温下氧气及水蒸气能明显腐蚀氮化硅。一种合成氮化硅的工艺主要流程如下:
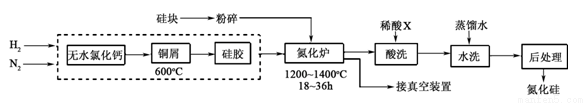
①净化N2和H2时,铜屑的作用是: ;硅胶的作用是 。
②在氮化炉中3SiO2(s)+2N2(g)=Si3N4(s) △H=-727.5kJ/mol,开始时为什么要严格控制氮气的流速以控制温度 ;体系中要通入适量的氢气是为了 。
③X可能是 (选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)。
(3)工业上可以通过如下图所示的流程制取纯硅:
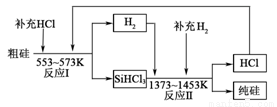
①整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应,写出该反应的化学方程式 。
②假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%。则在第二轮次的生产中,补充投入HCl 和H2的物质的量之比是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省商丘市高三上学期第二次模拟理综化学试卷(解析版) 题型:填空题
根据价层电子对互斥理论判断下列分子或离子中空间构型是V形的是 (填写序号)
a.H3O+ b.H2O c.NO2+ d.NO2﹣
(2)已知FeCl3的沸点:319℃,熔点:306℃,则FeCl3的晶体类型为 .P可形成H3PO4、HPO3、H3PO3等多种酸,则这三种酸的酸性由强到弱的顺序为 (用化学式填写)
(3)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2.T的基态原子外围电子(价电子)排布式为 Q2+的未成对电子数是 .
(4)如图1是从NaCl或CsCl晶体结构图中分割出来的部分结构图,判断NaCl晶体结构的图象是图1中的 .
(5)[Cu(NH3)4]2+配离子中存在的化学键类型有 (填序号).
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键,
若[Cu(NH3)4]2+具有对称的空间构型,且当[Cu(NH3)4]2+中的两个NH3被两个Cl﹣取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 (填序号)
①平面正方形②正四面体③三角锥形④V形.
(6)X与Y可形成离子化合物,其晶胞结构如图2所示.其中X和Y的相对原子质量分别为a和b,晶体密度为ρg/cm3,则晶胞中距离最近的X、Y之间的核间距离是 cm(NA表示阿伏伽德罗常数,用含ρ、a、b、NA的代数式表达)
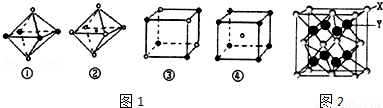
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com