


 ��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 nW(g)����H��ij��ѧ��ȤС���ͬѧ���ݴ˷�Ӧ�ڲ�ͬ�����µ�ʵ�����ݣ���������������ͼ��
nW(g)����H��ij��ѧ��ȤС���ͬѧ���ݴ˷�Ӧ�ڲ�ͬ�����µ�ʵ�����ݣ���������������ͼ��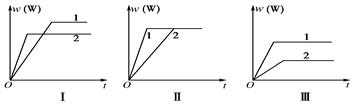
| A��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��p1>p2��a��b<n |
| B��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��p1>p2��n<a��b |
| C��ͼ���������ͬ��ͬѹ�²�ͬ�����Է�Ӧ��Ӱ�죬�Ң�ʹ�õĴ���Ч���� |
| D��ͼ������Dz�ͬ�¶ȶԷ�Ӧ��Ӱ�죬��T1>T2����H<0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ��֪��� | ʼ̬�����ʵ���(mol) | ƽ��ʱNH3�� ���ʵ�����mol�� | ||
| N2 | H2 | NH3 | ||
| ��֪ | 1 | 4 | 0 | a |
| �� | | | 1 | 0.5a |
| �� | 1.5 | 6 | 0 | |
| �� | m | n( n��4m) | | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g) ?H=-akJ/mol��a>0������2min�ﵽƽ��״̬����Ӧ����0.25akJ�������ж���ȷ����
2SO3(g) ?H=-akJ/mol��a>0������2min�ﵽƽ��״̬����Ӧ����0.25akJ�������ж���ȷ����| A����1minʱ��c��SO3��+c��SO2��="1.0" mol��L��1 |
| B����2min�ڣ�v��SO2��="0.25" mol��L��1��min-1 |
| C�����ٳ���2molSO3���ﵽƽ��ʱSO3������������С |
| D����Ӧ������ͬ������ʼʱ��Ӧ��������2molSO3���ﵽƽ��ʱ��Ӧ����0.75 akJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
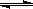 PCl3��g��+Cl2��g������ƽ������������г���amol PCl5���ٴδﵽƽ�����ԭƽ��Ƚϣ�������������ȷ���� �� ��
PCl3��g��+Cl2��g������ƽ������������г���amol PCl5���ٴδﵽƽ�����ԭƽ��Ƚϣ�������������ȷ���� �� ��| A�����������ܶ����� |
| B�����ƽ�������������� |
| C��PCl5��ת������� |
| D��PCl5�������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
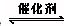 2SO3 ������һ������Ӧ���ȵĿ��淴Ӧ�������й�˵���д�����ǣ���
2SO3 ������һ������Ӧ���ȵĿ��淴Ӧ�������й�˵���д�����ǣ���| A��ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч�� |
| B�����������£�SO2������100��ת��ΪSO3�� |
| C���ﵽƽ��״̬ʱ��SO2Ũ����SO3Ũ����� |
| D���ﵽƽ��״̬ʱ��SO2������������SO2������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2HBr(g)���ﵽƽ��״̬������˵����һ����ȷ���� ����˵���˷�Ӧ�ﵽƽ��״̬���� ��
2HBr(g)���ﵽƽ��״̬������˵����һ����ȷ���� ����˵���˷�Ӧ�ﵽƽ��״̬���� ��| A����λʱ��������n mol H2��ͬʱ����2n mol HBr |
| B����λʱ��������n mol H2��ͬʱ����n molBr2 |
| C��һ��H��H�����ѵ�ͬʱ������H��Br������ |
| D����HBr�ݡã�H2�ݡã�Br2��=2��2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼŨ�Ⱦ�Ϊc(A)="0.100" mol��L-1,c(B)="0.200" mol��L-1, c(C)="0" mol��L-1����Ӧ��A��Ũ����ʱ��ı仯��ͼ��ʾ������˵����ȷ����
C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼŨ�Ⱦ�Ϊc(A)="0.100" mol��L-1,c(B)="0.200" mol��L-1, c(C)="0" mol��L-1����Ӧ��A��Ũ����ʱ��ı仯��ͼ��ʾ������˵����ȷ����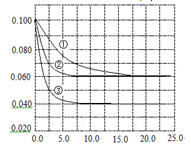
 C����H��0
C����H��0�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
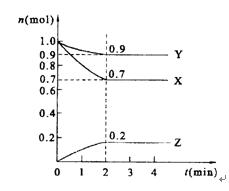
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com