
【题目】已知:HCN( aq)与NaOH(aq)反应的ΔH=-12.1 kJ·mol-1; HCl(aq)与NaOH(aq)反应的ΔH=-55. 6 kJ·mol-1。则HCN在水溶液中电离的ΔH等于
A.-67.7 kJ·mol-1 B.-43.5 kJ·mol-1
C.+43.5 kJ·mol-1 D.+67.7 kJ·mol-1
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,生成物总能量高于反应物总能量的是( )
A.乙醇燃烧B.氧化钙溶于水
C.Ba(OH)2·8H2O和NH4Cl固体反应D.锌粉和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和现象所得出的结论正确的是
选 项 | 实验操作 | 实验现象 | 结 论 |
A | 向NaHS溶液中滴入酚酞 | 溶液变红色 | HS-水解程度大于电离程度 |
B | 向浓度均为0.1 mol·L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]<Ksp[Cu(OH)2] |
C | 向Na2CO3溶液中加入浓盐酸,将产生的气体通入苯酚钠溶液中 | 产生白色浑浊 | 酸性:盐酸>碳酸>苯酚 |
D | 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液 | 前者溶液变蓝色,后者有黄色沉淀 | KI3溶液中存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V2O5是工业制硫酸的重要催化剂。V2O5及其含V离子在溶液中存在如下转化关系:

回答下列问题:
(1)从性质角度分类。V2O5属于_______(填“酸性”“碱性”或“两性”)氧化物,VO2+中钒元素的化合价为__________。
(2)写出反应Ⅰ的离子方程式:___________。
(3)向20mL 0.05mol/L (VO2)2SO4溶液中加入0.195g 锌粉,恰好完全反应,则还原产物中钒元素的存在形式为_________(填字母)。
a.V2+ b.V3+ c.VO2+ d.VO3-
(4)在酸性环境中,向含有VO2+的溶液中滴加草酸(H2C2O4)溶液,可实现反应Ⅲ的转化,写出该反应的离子方程式:__________。
(5)将V2O5加入浓盐酸中可得蓝色溶液,并有黄绿色气体生成,该反应中还原产物与氧化常务的物质的量之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氮的氧化物的说法中,正确的是
A. 氮的氧化物都是酸性氧化物
B. 氮的氧化物都既有氧化性,又有还原性
C. NO2 与 H2O 反应生成 HNO3,所以 NO2 是酸性氧化物
D. NO 和 NO2 均有毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“类推”这种思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中错误的是( )
①钠与水反应生成NaOH和H2 , 所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈,性质更活泼的铝不能稳定存在于空气中
③Cu(OH)2受热易分解,Fe(OH)3受热也易分解
④Al(OH)2能与NaOH反应,Be(OH)2也能与NaOH反应.
A.①③
B.②④
C.①②
D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计了一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:

(1)通入氧气的电极为_____(填“正极”或“负极”),写出负极的电极反应式_____.
(2)铁电极为_____(填“阳极”或“阴极”),石墨电极的电极反应式为_____.
(3)反应一段时间后,乙装置中生成NaOH主要在_____(填“铁极”或“石墨极”)区.
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为_____,反应一段时间,硫酸铜溶液浓度将_____(填“增大”“减小”或“不变”).
(5)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为_____;丙装置中阴极析出铜的质量为_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题: 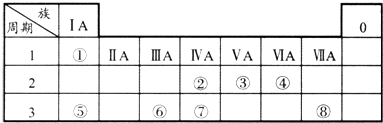
(1)④⑤⑥的简单离子半径由大到小的顺序为(填离子符号).
(2)②③⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式).
(3)④和⑤的单质常温可以反应生成化合物A,用电子式表示化合物A的形成过程
(4)①④⑤⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式 .
(5)由①④两种元素形成常见液态化合物,该化合物可使酸性高锰酸钾溶液褪色,写出该离子方程式 .
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应: 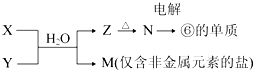
X溶液与Y溶液反应的离子方程式为 , 足量单质⑥与等物质的量的硫酸和氢氧化钠溶液反应生成氢气的物质的量之比为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com