
【题目】已知化学反应①: Fe(s)+CO2(g)═FeO(s)+CO(g),其平衡常数为K1;化学反应②:
Fe(s)+H2O(g)═FeO(s)+H2(g),其平衡常数为K2 . 在温度
973K和1173K情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973K | 1.47 | 2.38 |
1173K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是(填“吸热”或“放热”)反应.
(2)现有反应③:CO2(g)+H2(g)=CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3= .
(3)根据反应①与②可推导出K1、K2与K3之间的关系式 . 据此关系式及上表数据,也能推断出反应③是(填“吸热”或“放热”)反应,要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有(填写序号). A.缩小反应容器容积 B.扩大反应容器容积
C.降低温度 D.升高温度
E.使用合适的催化剂 F.设法减少CO的量
(4)图甲、乙分别表示反应③在t1时刻达到平衡、在t2时刻因改变某个条件而发生变化的情况: ①图甲中t2时刻发生改变的条件是 .
②图乙中t2时刻发生改变的条件是 . 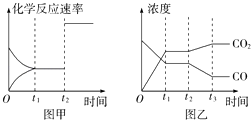
【答案】
(1)吸热
(2)![]()
(3)K3= ![]() ;吸热;DF
;吸热;DF
(4)加入催化剂或增大体系的压强;降低温度或增加水蒸气的量或减少氢气的量
【解析】解:(1)K1(973K时)<K1(1173K时),说明升高温度平衡正向移动,所以反应①是一个吸热反应,所以答案是:吸热;(2)反应③:CO2(g)+H2(g)=CO(g)+H2O(g)的平衡常数K3= ![]() , 所以答案是:
, 所以答案是: ![]() ;(3)反应③=反应①﹣反应②,则反应③的平衡常数K3=
;(3)反应③=反应①﹣反应②,则反应③的平衡常数K3= ![]() =
= ![]() =
= ![]() ,从表中数据可知,K1随温度升高增大,K2随温度升高减小,则随温度升高K3增大,说明升高温度平衡正向移动,反应③是吸热反应;
,从表中数据可知,K1随温度升高增大,K2随温度升高减小,则随温度升高K3增大,说明升高温度平衡正向移动,反应③是吸热反应;
A.缩小反应容器容积,压强增大,反应气体气体体积不变,平衡不移动,故A错误;
B.扩大反应容器容积,压强减小,反应气体气体体积不变,平衡不移动,故B错误;
C.正反应为吸热反应,降低温度,平衡向逆反应方向移动,故C错误;
D.正反应为吸热反应,升高温度,平衡向正反应方向移动,故D正确;
E.使用合适的催化剂,可以加快反应速率,但不影响平衡移动,故E错误;
F.设法减少CO的量,平衡向生成CO的方向移动,即平衡正向移动,故F正确,
所以答案是:K3= ![]() ;吸热;DF;(4)①从图甲可以看出,t2时刻平衡方向没有移动,化学反应速率加快,所以其条件是使用了催化剂;又因为反应③是反应前后气体体积不变的反应,所以增大压强,平衡不移动,反应速率也提高,
;吸热;DF;(4)①从图甲可以看出,t2时刻平衡方向没有移动,化学反应速率加快,所以其条件是使用了催化剂;又因为反应③是反应前后气体体积不变的反应,所以增大压强,平衡不移动,反应速率也提高,
所以答案是:加入催化剂或增大体系的压强;
②图乙中t2时刻后,CO2浓度增大,CO浓度减小,所以可以通过使平衡左移来达到,条件可以是降低温度,也可以采用增加水蒸气的量或者减少氢气的量,
所以答案是:降低温度或增加水蒸气的量或减少氢气的量.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】通过加入适量的化学药品,采用恰当的分离提纯方法,除去某溶液里溶解的杂质,下列做法中不正确的是(括号内的物质为杂质)
A | NaCl溶液(BaCl2) | 加Na2CO3溶液,过滤,再加适量盐酸 |
B | KNO3溶液(AgNO3) | 加适量KCl溶液,过滤 |
C | NaCl溶液(I2) | 加酒精,分液 |
D | KNO3溶液(I2) | 加CCl4,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,固定容积的容器中加入a mol A和b mol B,发生反应:A(g)+2B(g)2C(g)一段时间后达到平衡,生成n mol C.则下列说法中不正确的是( )
A.再充入少量A,平衡向正反应方向移动,但K值不变
B.起始时刻和达到平衡后容器中的压强之比为(a+b):(a+b﹣ ![]() )
)
C.当2v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar)增大压强,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸、硫代硫酸(H2S2O3) 等等,其中硫酸最为重要,在工业上有广泛的应用,在实验室,浓硫酸是常用的干燥剂.
(1)焦硫酸(H2SO4SO3)溶于水,其中的SO3都转化为硫酸,若将890g焦硫酸溶于水配成8.00L硫酸,该硫酸的物质的量浓度=molL﹣1;
(2)若以浓硫酸吸水后生成H2SO4H2O计算,500g质量分数为98%的硫酸能吸收水的质量= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni﹣Cd)可充电电池在现代生活中有广泛应用.电解质溶液为KOH溶液,电池反应为:Cd+2NiO(OH)+2H2O ![]() Cd(OH)2+2Ni(OH)2 , 下列有关镍镉电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2 , 下列有关镍镉电池的说法正确的是( )
A.充电过程是化学能转化为电能的过程
B.充电时阳极反应为Cd(OH)2+2e﹣═Cd+2OH ﹣
C.放电时电池内部OH﹣向正极移动
D.充电时与直流电源正极相连的电极上发生Ni(OH)2转化为NiO(OH)的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.100 0molL﹣1盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:
(1)配制待测液:用2.50g含有少量杂质的固体烧碱样品配制500mL溶液.需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要 .
(2)滴定: Ⅰ.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“0”刻度线以上.
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”或“0”刻度线以下,并记录读数.
Ⅲ.移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液.
Ⅳ.用标准液滴定至终点,记录滴定管液面读数.
①上述滴定步骤中有错误的是(填编号) , 该错误操作会导致测定结果
(填“偏大”“偏小”或“无影响”).
②步骤Ⅳ中滴定时眼睛应 , 判断滴定终点的现象是 .
③若步骤Ⅱ中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果(填“偏大”“偏小”或“无影响”).
(3)按正确操作测得有关数据记录如下:
滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 20.00 | 0.20 | 20.38 |
第二次 | 20.00 | 4.00 | 24.20 |
第三次 | 20.00 | 2.38 | a |
①a的读数如图所示,则a=;
②烧碱样品的纯度为%.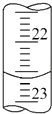
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法正确的是( )
A.将饱和硫酸铜溶液降温,析出的固体不是晶体
B.假宝石往往是玻璃仿造的,可以用划痕的方法鉴别宝石和玻璃制品
C.石蜡和玻璃都是非晶体,但它们都有固定的熔点
D.蓝宝石在不同方向上的硬度一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值.下列说法中正确的是( )
A.标准状况下,22.4L酒精中含有的分子数目为NA
B.常温常压下,1.0mol/L盐酸中含有的氯离子数目为NA
C.常温常压下,24gO2和24gO3含有的氧原子数目都为1.5NA
D.标准状况下,2.24L氯气与足量NaOH溶液反应转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2与N2O4相互转化:2NO2(g)N2O4(g);△H=﹣24.2kJ/mol 在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图.下列推理分析合理的是( )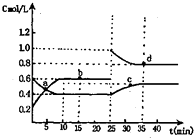
A.a,b,c,d四点中c正与v逆均相等
B.反应进行到10min时,体系吸收的热量为9.68kJ
C.前10min内,用v(NO2)表示的该反应速率为0.02mol/Lmin
D.25min时,导致平衡移动的原因是升温
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com