
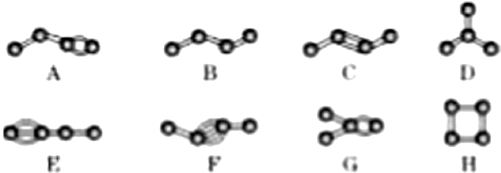
分析 (1)碳碳之间以单键相连且为链状的烃为烷烃;
(2)这几种物质中都含有4个碳原子,相同碳原子的烃不饱和度越大的其含有H原子个数越少;
(3)分子式相同结构不同的有机物互称同分异构体.
解答 解:(1)碳碳之间以单键相连且为链状的烃为烷烃,根据图知,只有BD中只含碳碳单键且为链状,所以属于烷烃,故答案为:BD;
(2)这几种物质中都含有4个碳原子,相同碳原子的烃不饱和度越大的其含有H原子个数越少,根据图知,ACGH的不饱和度是1、BD的不饱和度是0、EF的不饱和度是2,所以分子中氢原子数最少的是EF,故答案为:EF;
(3)分子式相同结构不同的有机物互称同分异构体,BD分子式相同其结构不同,为同分异构体;ACGH分子式相同而结构不同属于同分异构体;EF分子式相同而结构不同,为同分异构体,所以有3种同分异构体,故答案为:3.
点评 本题考查有机化学基础知识,涉及同分异构体判断、基本概念及碳原子成键特征等知识点,明确基本概念内涵及碳原子成键特点是解本题关键,烃CxHy中不饱和度公式=$\frac{2x+2-y}{2}$,双键和环的不饱和度是1、三键的不饱和度是2,知道不饱和度的计算方法,题目难度不大.


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:选择题
| A. | 石油大体上是由各种碳氢化合物组成的混合物 | |
| B. | 石油分馏得到的各馏分是由各种碳氢化合物组成的混合物 | |
| C. | 石油裂解和裂化的主要目的都是为了得到重要产品乙烯 | |
| D. | 实验室里,在氧化铝粉末的作用下,用石蜡可以制出汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 古代发明 | 化学变化 |
| A | 生产陶瓷 | SiO2+CaCO3 $\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑ |
| B | 黑火药爆炸 | S+2KNO3+3C$\frac{\underline{\;点燃\;}}{\;}$K2S+N2↑+3CO2↑ |
| C | 湿法炼铜 | CuSO4+Fe═Cu+FeSO4 |
| D | 用谷物酿酒 | (C6H10O5)n→C6H12O6→CH3CH2OH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲基中含电子数目为10NA | |
| B. | 标准状况下,11.2L己烷所含有的分子数为0.5NA | |
| C. | 14g乙烯和丁烯的混合物中含有的原子总数为3NA个 | |
| D. | 常温下,4gCH4含有2NA个C-H共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
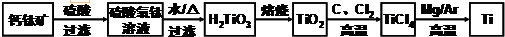
 ,其原子核外共有22种运动状态不相同的电子.金属钛晶胞如图1所示,为六方最密堆积(填堆积方式).
,其原子核外共有22种运动状态不相同的电子.金属钛晶胞如图1所示,为六方最密堆积(填堆积方式).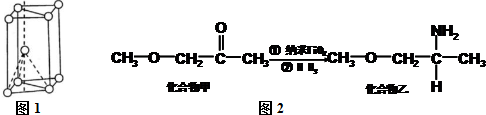

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
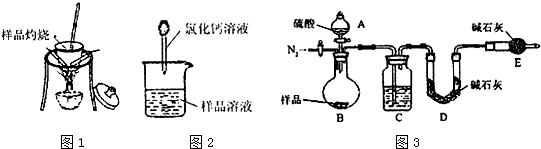
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可逆反应的化学反应速率是指正反应速率 | |
| B. | 在可逆反应里正反应的速率是正值,逆反应的速率是负值 | |
| C. | 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度 | |
| D. | 对于可逆反应来说,反应物转化为生成物没有一定的限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
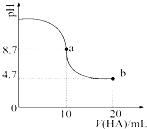 室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的
室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的| A. | a点所示溶液中c(HA)>c(A-) | |
| B. | a点所示溶液中c(Na+)=c(A-)+c(HA) | |
| C. | 当加入HA溶液10ml时,$\frac{{K}_{w}}{c({H}^{+})}$<1.0×10-7mol•L-1 | |
| D. | b点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使石蕊试液变红 | |
| B. | 与铜反应生成Cu(NO3)2和NO气体 | |
| C. | 与Na2CO3反应放出CO2气体生成NaNO3 | |
| D. | 与C单质混合共热时生成CO2和NO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com