
��5��)������ʵ������ȡ���峣�õĻ�ѧ������
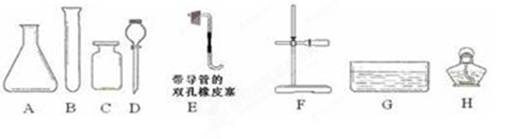
��ش��������⣺
��1�������F������ ��
��2��д��ʵ������˫��ˮ�Ͷ���������ȡ�����Ļ�ѧ����ʽ ����ȡ��������������ˮ���ռ�ʱ���ѡ��������Щ���� ������ĸ����
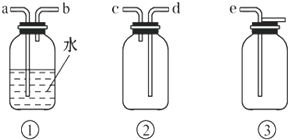
��3������˿�������е�ȼ��ʵ��ʱ���ڼ���ƿ�ײ�������ˮ��Ŀ���ǣ� ��
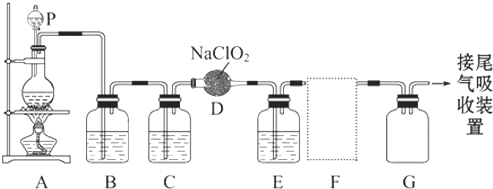
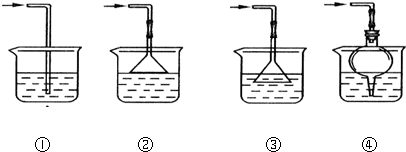
��4��ʵ����ͨ����������ͼ��ʾ��ϴ��װ�ö��������и��������װ��ҩƷ������ ������ĸ����
A��Ũ���� B������������Һ C����ʯ�� D���Ȼ��ƹ���
��1������̨
��2��2H2O2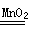 2H2O+O2�� ACDEG��BCDEFG
2H2O+O2�� ACDEG��BCDEFG
��3����ֹ���ɵĸ���������ը�Ѽ���ƿ ��4��A
����������1������F�Ĺ����֪��F������̨��
��2��˫��ˮ���ȶ����ֽ����������ˮ������ʽΪ2H2O2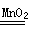 2H2O+O2�������ڸ÷�Ӧ����Ҫ���ȣ����H����Ҫ��������ȷ��ѡ����ACDEG��BCDEFG��
2H2O+O2�������ڸ÷�Ӧ����Ҫ���ȣ����H����Ҫ��������ȷ��ѡ����ACDEG��BCDEFG��
��3����˿��������ȼ���зų��������ȣ������ڼ���ƿ�ײ�������ˮ��Ŀ���Ƿ�ֹ���ɵĸ���������ը�Ѽ���ƿ��
��4��������������Ũ���������������ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 |
| CuSO4?5H2O | 23.1 | 32.0 | 44.6 | 61.8 | 83.8 | 114.0 |
| Cu��NO3��2?xH2O | 83.5 | 125.0 | 163.0 | 182.0 | 208.0 | 247.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�긣��ʡ�������и�һ������ѧ���Ի�ѧ�Ծ����������� ���ͣ�ʵ����
��5��)������ʵ������ȡ���峣�õĻ�ѧ������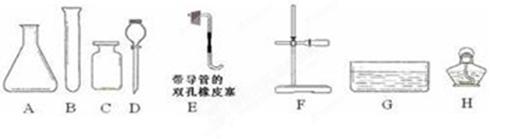
��ش��������⣺
��1�������F������ ��
��2��д��ʵ������˫��ˮ�Ͷ���������ȡ�����Ļ�ѧ����ʽ ����ȡ��������������ˮ���ռ�ʱ���ѡ��������Щ���� ������ĸ����
��3������˿�������е�ȼ��ʵ��ʱ���ڼ���ƿ�ײ�������ˮ��Ŀ���ǣ� ��
��4��ʵ����ͨ����������ͼ��ʾ��ϴ��װ�ö��������и��������װ��ҩƷ������ ������ĸ����
| A��Ũ���� | B������������Һ | C����ʯ�� | D���Ȼ��ƹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�츣��ʡ�����и�����һѧ����ĩ������鿼�Ի�ѧ�Ծ� ���ͣ�ʵ����
(16��)��ȸʯ����Ҫ�ɷ�ΪCu2(OH)2CO3���������������������������������ʵ�����Կ�ȸʯΪԭ���Ʊ�CuSO4��5H2O���������ͼ��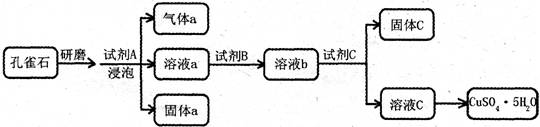
(1)��ȸʯ��ĥ��Ŀ���� �����ݿ�ȸʯ���Լ�A��ѡ�ù�����ϡ���ᣬ�����������a�� (�ѧʽ)������a�� (�ѧʽ)��
(2)ʹ���Լ�B��Ŀ���ǽ���Һ�е�Fe2+ת��ΪFe3+���Լ�B��ѡ�� (��ѡ�����)��
A������KMnO4��Һ B��˫��ˮ C��Ũ���� D����ˮ
��Ӧ�Ļ�ѧ��Ӧ����ʽ�� ��
(3)�Լ�C��ʹ��Ŀ���ǵ�����ҺpH��ʹFe3+ת��Ϊ�������Է��롣�Լ�C��ѡ�� (��ѡ�����)��
A��ϡ���� B��NaOH��Һ C����ˮ D��CuO
��Ӧ�����ӷ���ʽ ��
(4)1 mol����ͨ�����ȵ�Cu2(OH)2 CO3���Բ���1.5 mol����ͭ��������Ӧ�Ļ�ѧ����
ʽ�� ��
(5)������Fe(OH)3��Ksp=1��10-39����Ҫ����Һ�е�Fe3+ת��ΪFe(OH)3������ʹ��Һ��c(Fe3+)������1��10��3 mol��L�����轫��ҺpH������ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com