
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g)2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是 ( )。
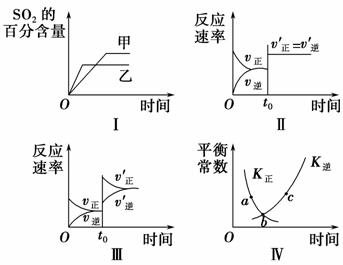
A.图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态
科目:高中化学 来源: 题型:
PbO2是褐色固体,受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1 mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为3∶2。则剩余固体的组成及物质的量之比是 ( )。
A.1∶1混合的Pb3O4、PbO
B.1∶2混合的PbO2、Pb3O4
C.1∶4∶1混合的PbO2、Pb3O4、PbO
D.1∶4∶1混合的PbO2、Pb3O4、PbO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于油、脂、矿物油的说法中,不正确的是( )
A.油是不饱和高级脂肪酸的单甘油酯,是纯净物
B.脂是高级脂肪酸中含饱和烃基较多的混甘油酸,脂属于酯类
C.油和脂是由于含饱和烃基和不饱和烃基的相对含量不同引起熔点不同进行区分的
D.区分植物油和矿物油可采用加入NaOH溶液加热的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积可变的密闭容器中,1 mol N2和4 mol H2在一定条件下发生反应,达到平衡时,H2的转化率为25%,则平衡时的氮气的体积分数接近于 ( )。
A.5% B.10%
C.15% D.20%
查看答案和解析>>
科目:高中化学 来源: 题型:
在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表:
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是 ( )。
A.上述生成Ni(CO)4的反应为放热反应
B.25 ℃时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10-5
C.在80 ℃时,测得某时刻Ni(CO)4、CO的浓度均为0.5 mol·L-1,则此时
v正>v逆
D.80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol
·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
密闭容器中进行的可逆反应:aA(g)+bB(g)cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是 ( )。

A.T1<T2,p1<p2,a+b>c,正反应为吸热反应
B.T1>T2,p1<p2,a+b<c,正反应为吸热反应
C.T1<T2,p1>p2,a+b<c,正反应为吸热反应
D.T1>T2,p1>p2,a+b>c,正反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是 ( )。
A.化学变化过程是原子的重新组合过程
B.根据化学反应中的能量变化情况,化学反应可分为吸热反应和放热反应
C.化学反应中的能量变化多少与其反应物用量有关
D.化学反应中的能量变化都是以热能形式表现出来的
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2(g)+Cl2(g)===2HCl(g) ΔH=-184.6 kJ·mol-1,则反应:HCl(g)===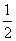 H2(g)+
H2(g)+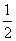 Cl2(g)的ΔH为 ( )。
Cl2(g)的ΔH为 ( )。
A.+184.6 kJ·mol-1 B.-92.3 kJ·mol-1
C.-369.2 kJ·mol-1 D.+92.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
乙烯催化氧化成乙醛可设计成如右图所示的燃料电池,
能在制备乙醛的同时获得电能,其总反应为:
2CH2=CH2 +O2→2CH3CHO。下列有关说法正确的是
A.每有0.1mol O2反应,则迁移H+ 0.4mol
B.正极反应式为:CH2=CH2-2e- + 2OH- = CH3CHO + H2O
C.电子移动方向:电极a→磷酸溶液→电极b D.该电池为可充电电池
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com