
| A. | 将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+) | |
| B. | 为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 | |
| C. | pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | |
| D. | 向0.1 mol•L-1的氨水中加入少量硫酸铵固体,则溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 |
分析 A.结合溶液中电荷守恒判断;
B.NaHA溶液若PH>7说明溶液呈碱性,说明对应酸一定为弱酸,若pH<7可能对应酸是强酸,也可能对应酸是弱酸;
C.氢氧化钠是强电解质,醋酸是弱电解质,在溶液中存在电离平衡,pH=11的NaOH溶液与pH=3的醋酸溶液中,醋酸浓度大于氢氧化钠,等体积混合酸有剩余;
D.一水合氨是弱电解质,存在电离平衡,向氨水中加入醋酸铵,抑制一水合氨电离.
解答 解:A.混合溶液呈中性,所以c(H+)=c(OH-),根据电荷守恒得c(NH4+)+c(H+)=c(OH-)+2c(SO42-),所以c(NH4+)>c(SO42-),故A错误;
B.NaHA溶液若pH>7说明溶液呈碱性,说明对应酸一定为弱酸,若pH<7可能对应酸是强酸,如硫酸氢钠,也可能对应酸是弱酸,如亚硫酸氢钠,故B错误;
C.pH=11的NaOH溶液与pH=3的醋酸溶液中,醋酸浓度大于氢氧化钠,等体积混合酸有剩余,溶液呈酸性,石蕊试液遇酸变红色,故C正确;
D.一水合氨是弱电解质,存在电离平衡,向氨水中加入醋酸铵,抑制一水合氨电离,溶液中氢氧根离子浓度减小,一水合氨浓度增大,所以氢氧根离子浓度与一水合氨浓度的比减小,故D错误;
故选C.
点评 本题考查了弱电解质的电离,明确弱电解质电离特点、pH与氢离子浓度的换算、弱电解质电离程度与浓度的关系是解本题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
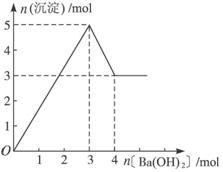 如图表示在某溶液中滴加Ba(OH) 2溶液时,沉淀的物质的量随Ba(OH) 2的物质的量的变化关系.该溶液的成分可能是( )
如图表示在某溶液中滴加Ba(OH) 2溶液时,沉淀的物质的量随Ba(OH) 2的物质的量的变化关系.该溶液的成分可能是( )| A. | MgSO 4 | B. | Al 2(SO 4) 3 | C. | Fe 2(SO 4) 3 | D. | NaAlO 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol羟基含10 NA个电子 | |
| B. | 标准状况下,11.2L四氯化碳所含分子总数为0.5NA | |
| C. | 1 mol聚乙烯含有的原子总数目为6NA | |
| D. | 20℃时,2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应进行30s时,正反应速率等于逆反应速率 | |
| B. | 反应进行80s时,逆反应速率大于正反应速率 | |
| C. | 前60 s,以X浓度变化表示的平均反应速率为0.0005mol/(L•s) | |
| D. | 反应进行80s时,X物质的量浓度为0.04mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a-4 | B. | a+3 | C. | a+3 | D. | a+4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•xH2O)是一种光敏材料,110℃时失去全部结晶水.某实验小组为测定该晶体中铁的含量,做了如下实验,完成下列填空:
三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•xH2O)是一种光敏材料,110℃时失去全部结晶水.某实验小组为测定该晶体中铁的含量,做了如下实验,完成下列填空:| 滴定次数 | 滴定起始读数(mL) | 滴定终点读数(mL) |
| 第一次 | 1.08 | 见右图 |
| 第二次 | 2.02 | 24.52 |
| 第三次 | 1.00 | 20.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液.
实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C、D、E、F六种中学常见的物质,皆有短周期元素组成,有转化关系:
A、B、C、D、E、F六种中学常见的物质,皆有短周期元素组成,有转化关系:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com