
分析 Na2O和H2SO4溶液反应的化学方程式为Na2O+H2SO4=Na2SO4+H2O,3.1g氧化钠的物质的量为$\frac{3.1g}{62g/mol}$=0.05mol,则需要硫酸的物质的量为0.05mol,生成硫酸钠的物质的量为0.05mol,据此分析.
解答 解:3.1g氧化钠的物质的量为$\frac{3.1g}{62g/mol}$=0.05mol,据Na2O+H2SO4=Na2SO4+H2O可知,需要硫酸的物质的量为0.05mol,其物质的量浓度为$\frac{0.05mol}{0.05L}$=1mol/L,生成硫酸钠的质量为0.05mol×142g/mol=7.1g,故答案为:1;7.1.
点评 本题考查了物质的量浓度以及物质的量与质量的相互换算,注意M、NA、Vm的含义和应用.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:推断题
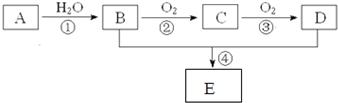
 ,B、D分子中的官能团名称分别是羟基、羧基.
,B、D分子中的官能团名称分别是羟基、羧基. CH3COOCH2CH3+H2O,取代反应或酯化反应.
CH3COOCH2CH3+H2O,取代反应或酯化反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl Na2CO3 NH4Cl NaHSO4 | |
| B. | NaHSO4 NH4Cl NaCl Na2CO3 | |
| C. | NH4Cl NaHSO4 NaCl Na2CO3 | |
| D. | Na2CO3 NaCl NH4Cl NaHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取8.84 g食盐 | |
| B. | 用220 mL容量瓶配制所需的220 mL 0.1 mol/L NaOH溶液 | |
| C. | 用量筒量取12.12 mL盐酸 | |
| D. | 用0.1200 mol/L盐酸滴定未知浓度的NaOH溶液,消耗盐酸21.40 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
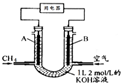 将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL.完成下列问题:
将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL.完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(O2)=0.225 mol•L-1min-1 | B. | v(H2O)=0.375 mol•L-1min-1 | ||
| C. | v(N2)=0.125 mol•L-1min-1 | D. | v(NH3)=0.250 mol•L-1min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
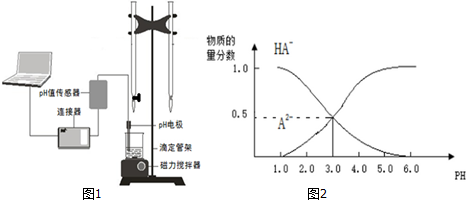
| A. | pH=4.0时,图中n(HA-)约为0.0091mol | |
| B. | 该实验应将左边的酸式滴定管换成右边碱式滴定管并加酚酞作指示剂 | |
| C. | 常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0 | |
| D. | 0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com