
某容器中发生一个化学反应,反应过程中存在H2O、ClO-、 NH3、N2、Cl-五种物质,在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是 ( )
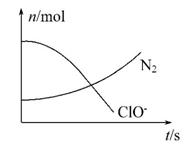
A.还原剂是NH3,氧化产物是Cl-
B.配平后氧化剂与还原剂的化学计量数之比为3∶2
C.该反应中氧化反应过程是ClO-→Cl-
D.标准状况下,若生成2.24 L N2,则转移电子为0.5 mol
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:
向有机物X中加入合适的试剂(可以加热),检验其官能团。下列有关结论错误的是
| 选项 | 试剂 | 现象 | 结论 |
| A | 金属钠 | 有气体产生 | 含羟基或羧基或羟基、羧基 |
| B | 银氨溶液 | 产生银镜 | 含有醛基 |
| C | 碳酸氢钠溶液 | 产生气泡 | 含有羧基 |
| D | 溴水 | 溶液褪色 | 含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与环境保护密切相关,下列叙述正确的是( )
A.绿色化学的核心是应用化学原理对环境污染进行治理
B.处理废水时加入明矾作为消毒剂对水进行杀菌消毒。
C.PM2.5(2.5微米以下的细颗粒物)主要来自化石燃料的燃烧
D.某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多
的CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求填空
(1)二氧化硫气体通入碘水,碘水褪色,该反应的化学方程式
(2)实验室制备氨气的化学方程式
(3)制备漂白粉的化学方程式
(4)收集满一烧瓶纯的二氧化氮气体做喷泉实验,假设溶液不扩散,所得溶液的物质的量浓度
(5)金属锌和硝酸物质的量之比为2:5恰好完全反应,该反应的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.Na2O2+2HCl====2NaCl+H2O2
B.Ag2O+H2O2====2Ag+O2↑+H2O
C.2H2O2====2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH====2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2仅体现氧化性的反应是(填序号,下同) ,H2O2既体现氧化性又体现还原性的反应是 。
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是 。
(3)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
O2、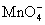 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
①反应体系选择的酸是: (填序号)。
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
②如果上述反应中有6.72 L(标准状况)气体生成,转移的电子为 mol。
(4)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应:KCN+H2O2+H2O====A+NH3↑,试指出生成物A的化学式为 ,并阐明H2O2被称为绿色氧化剂的理由是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在一个容积为1 L的密闭容器中,充入1 mol H2(g)和1 mol I2(g),发生反应H2(g)+I2(g) 2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,在该温度下,在另一个容积为2 L的密闭容器中充入1 mol HI(g)发生反应HI(g)
2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,在该温度下,在另一个容积为2 L的密闭容器中充入1 mol HI(g)发生反应HI(g)
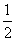 H2(g)+
H2(g)+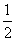 I2(g),则下列判断正确的是( )
I2(g),则下列判断正确的是( )
A.后一反应的平衡常数为1
B.后一反应的平衡常数为0.5
C.后一反应达到平衡时,H2的平衡浓度为0.25 mol·L-1
D.后一反应达到平衡时,HI(g)的平衡浓度为0.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F六种物质有如下变化关系,E是淡黄色粉末,判断:
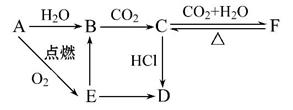
(1)写出A、B、C、D、E、F的化学式:
A. ;B. ;C. ;
D. ;E. ;F. 。
(2)写出有关反应的化学方程式(是离子反应的直接写出离子方程式)
B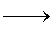 C: ___________________________________________________,
C: ___________________________________________________,
E B: __________________________________________________,
B: __________________________________________________,
C F: __________________________________________________,
F: __________________________________________________,
F C: __________________________________________________。
C: __________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组利用图一装置制取氨气并探究氨气的有关性质。
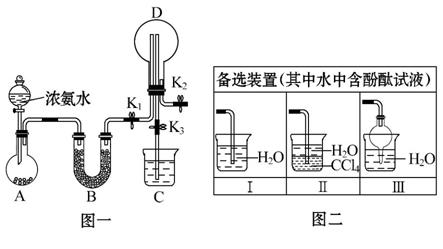 (1)装置A中烧瓶内试剂可选用 (填序号)。
(1)装置A中烧瓶内试剂可选用 (填序号)。
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱
(2)若探究氨气的溶解性,需在K2的导管末端连接图二装置中的 装置(填序号),当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是____
___________________________________________________________________。
(3)若探究氨气的还原性,需打开K1、K3,K2处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成气体必须通过盛有 试剂的洗气瓶;
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为 ;
③从K3处导管逸出的气体中含有少量Cl2,则C装置中应盛放 溶液(填化学式),反应的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com