
已知反应3X(g)+Y(g)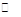 2Z(g) ΔH>0,T℃时化学平衡常数K = 2,在密闭容器中反应达到平衡,下列说法正确的是( )
2Z(g) ΔH>0,T℃时化学平衡常数K = 2,在密闭容器中反应达到平衡,下列说法正确的是( )
| A.升高温度平衡常数K减小 |
| B.若压缩体积,平衡向气体体积增大方向移动,混合气体的平均相对分子质量减小 |
| C.保持体积不变,通入稀有气体,压强增大,平衡向正反应方向移动 |
| D.T℃时,向2L密闭容器中加入 2molX、3molY、4molZ,反应将向左进行 |
科目:高中化学 来源: 题型:阅读理解
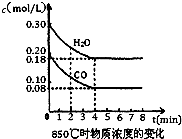 已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.
已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源:101网校同步练习 高一化学 山东科学技术出版社 鲁教版 题型:013
|
把0.6 mol气体X和0.4 mol气体Y混合于2.0 L的密闭容器中,发生如下反应3X(g)+Y(g) | |
| [ ] | |
A. |
1 |
B. |
2 |
C. |
3 |
D. |
4 |
查看答案和解析>>
科目:高中化学 来源:2013届重庆市高二上学期期末考试化学试卷 题型:选择题
已知反应3X(g)+Y(g) 2Z(g)
ΔH>0,T℃时化学平衡常数K = 2, 在密闭容器中反应达到平衡,下列说法正确的是( )
2Z(g)
ΔH>0,T℃时化学平衡常数K = 2, 在密闭容器中反应达到平衡,下列说法正确的是( )
A.升高温度平衡常数K减小
B.若压缩体积,平衡向气体体积增大方向移动,混合气体的平均相对分子质量减小
C.保持体积不变,通入稀有气体,压强增大,平衡向正反应方向移动
D.T℃时,向2L密闭容器中加入 2molX、3molY、4molZ,反应将向左进行
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应3X(g)+Y(g)![]() 2Z(g) ΔH>0,T℃时化学平衡常数K = 2, 在密闭容器中反应达到平衡,下列说法正确的是( )
2Z(g) ΔH>0,T℃时化学平衡常数K = 2, 在密闭容器中反应达到平衡,下列说法正确的是( )
A.升高温度平衡常数K减小
B.若压缩体积,平衡向气体体积增大方向移动,混合气体的平均相对分子质量减小
C.保持体积不变,通入稀有气体,压强增大,平衡向正反应方向移动
D.T℃时,向2L密闭容器中加入 2molX、3molY、4molZ,反应将向左进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com