
氢气是重要而洁净的能源,要利用氢气作能源,必须安全有效地储存氢气。有报道称某种合金材料有较大的储氢容量,其晶体结构的最小单元如右图所示,则这种合金的化学式为( )
A.LaNi6 B.LaNi3 C. LaNi4 D. LaNi5
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
下表是元素周期表的一部分,回答有关问题:
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ⑴ | ⑵ | ||||||
| 三 | ⑶ | ⑷ | ⑸ | ⑹ | ⑺ | ⑻ | ⑼ | |
| 四 | ⑽ | ⑾ | ⑿ |
(1)写出下列元素符号:⑴ ,⑹
(2)在这些元素中,最不活泼的元素的结构示意图是 。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的与呈两性的发生反应的化学方程式为 ;碱性最强的与呈两性的发生反应的离子方程式为 .
(4)在⑵⑶⑻⑽这些元素简单离子中,离子半径由大到小的顺序是 (填离子符号)
(5)元素⑻、⑾和氧元素形成一种广泛使用杀菌消毒剂,该物质中存在的化学键有 。(2分)
(6)用电子式表示由元素(8)和(10)形成化合物的过程: 。(2分)
查看答案和解析>>
科目:高中化学 来源: 题型:
湖南省常德市石门县鹤山村用土法炼砒霜导致地下水砷污染严重,157人中毒死亡。关于砷(33As)的说法不正确的是
A.砷的氢化物和磷的氢化物的稳定性为PH3<AsH3
B.砷原子核内有33个质子
C.砷是第四周期第VA族
D.砷的最高价氧化物对应的水化物的化学式是H3AsO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.CO2、BF3、PCl3分子中所有原子的最外层电子都满足8电子稳定结构
B.P4和CH4都是正四面体分子且键角都为109o28ˊ
C.乙烯分子有5个σ键,1个π键
D.丙烯分子中3个碳原子都是sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
某化肥厂用H2O、CO2、 NH3、CaSO4、制备(NH4)2SO4,工艺流程如下:
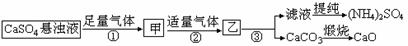
下列推断中正确的是( )
A.步骤①和②中的气体属于可循环使用的气体
B.步骤②中发生的反应为:Ca2++CO2+2NH3·H2O =CaCO3↓+2NH4++H2O
C.往甲中通CO2有利于(NH4)2SO4生成 D.以上涉及的化学反应中有氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
水能与多种金属离子形成络合物,某红紫色络合物的组成为CoCl3·5NH3·H2O。其水溶液显弱酸性,加入强碱加热至沸腾有氨放出,同时产生Co2O3沉淀;加AgNO3于该化合物溶液中,有AgCl沉淀生成,过滤后加AgNO3溶液于滤液中无变化,但加热至沸腾有AgCl沉淀生成, 且其质量为第一次沉淀量的二分之一。则该配合物的化学式最可能为( )
A.[ CoCl2(NH3)4 ]Cl·NH3·H2O B.[ Co(NH3)5(H2O)]Cl3
C.[ CoCl2(NH3)3(H2O)]Cl·2NH3 D.[ CoCl(NH3)5]Cl2·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是 ( )。
A.Na2O2用作呼吸面具的供氧剂
B.NaHCO3的热稳定性大于Na2CO3
C.乙醇可与金属钠反应放出氢气
D.金属钠着火时,可用细沙覆盖灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列各项叙述中正确的有
( )。
①0.2 mol H2O2完全分解转移的电子数为0.4NA
②25 ℃、101 kPa下,16 g O3和O2混合气体中含有的氧原子数为NA
③将含0.1 mol FeCl3的 饱和溶液滴入沸水形成的胶体粒子的数目为0.1NA
饱和溶液滴入沸水形成的胶体粒子的数目为0.1NA
④1 mol N2和3 mol H2在一定条件下的密闭容器中充分反应,容器内的分子数大于2NA
A.①②③ B.①②④ C.①②③④ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族.
(1)D在周期表中的位置 ;B的原子核外电子排布示意图 ;
(2)E元素形成最高价氧化物对应水化物对应的水化物的化学式为 ;
(3)元素C、D、E形成的原子半径大小关系是 (用元素符号表示)。
(4)C、D可形成化合物D2C2,D2C2含有的化学键是 ;
(5)A、C两种元素形成的原子个数之比为1:1的化合物电子式 ,
(6)B的氢化物与B的最高价氧化物的水化物反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com