
对于可逆反应N2(g)+3H2(g)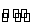 2NH3(g)(正反应为放热反应),下列说法中正确的是( )
2NH3(g)(正反应为放热反应),下列说法中正确的是( )
A.达到平衡后加入N2,当重新达到平衡时,NH3的浓度比原平衡的大,H2的浓度比原平衡的小
B.达到平衡后,升高温度,既加快了正、逆反应速率,又提高了NH3的产率
C.达到平衡后,缩小容器体积,既有利于加快正、逆反应速率,又有利于提高氢气的转化率
D.加入催化剂可以缩短达到平衡的时间,是因为正反应速率增大了,而逆反应速率减小了
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
常温下,向10 mL 0.1 mol·L-1的H2C2O4溶液中逐滴加入0.1 mol·L-1 KOH溶液,所得滴定曲线如图所示。下列说法正确的是
A.KHC2O4溶液呈弱碱性
B.B点时:c(K+)>c(HC2O4-)> c(C2O42-)>c(H+)>c(OH-)
C.C点时:c(K+)>c(HC2O4-)+c(C2O42-)+c(H2C2O4)
D.D点时:c(H+)+c(HC2O4-)+c(H2C2O4)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于原子半径和第一电离能的变化趋势的叙述中,正确的是
A.同周期元素的原子半径随着核电荷数的增大而增大
B.同主族元素的原子半径随着核电荷数的增大而增大
C.同周期元素的第一电离能随着核电荷数的增大而增大
D.同主族元素的第一电离能随着核电荷数的增大而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为 ;
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为 ,C的元素符号为 。用惰性电极电解B、C两元素组成的化合物的水溶液的化学方程式为 。
(3)D元素的正三价离子的3d轨道为半充满,D的元素符号为 ,其基态原子的价电子排布图为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
448 mL某气体在标准状况下的质量为0.64 g,该气体的摩尔质量约为( )
A.64 g B.64 C.64 g·mol-1 D.32 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,向密闭容器中充入1.0 mol N2和3.0 mol H2,反应达到平衡时,测得NH3的物质的量为0.6 mol。若该容器中开始时N2的物质的量为2.0 mol,H2为6.0 mol,则平衡时NH3的物质的量为( )
A.若为定容容器,n(NH3)=1.2 mol
B.若为定容容器,n(NH3)<1.2 mol
C.若为定压容器,n(N H3)=1.2 mol
H3)=1.2 mol
D.若为定压容器,n(NH3)>1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,1 mol/L的NH4Cl、CH3COONH4、NH4HSO4三种溶液中,测得c(NH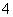 )分别为a、b、c(单位为mol/L),下列判断正确的是 ( )
)分别为a、b、c(单位为mol/L),下列判断正确的是 ( )
A.a=b=c B.a>b>c C.a>c>b D.c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2===Na2S2O5。

(1)装置Ⅰ中产生气体的化学方程式为________________________________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是__________________________。
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为__________(填序号)。
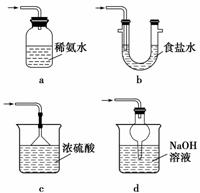
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO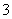 的电离程度大于水解程度,可采用的实验方法是________(填序号)。
的电离程度大于水解程度,可采用的实验方法是________(填序号)。
a.测定溶液的pH
b.加入Ba(OH)2溶液
c.加入盐酸
d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
 Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2====2Na2FeO4+2Na2O+2 +O2↑。下列对此反应的说法中,不正确的是( )
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2====2Na2FeO4+2Na2O+2 +O2↑。下列对此反应的说法中,不正确的是( )
A.方框中的物质为Na2SO4
B.Na2O2既是氧化剂,又是还原剂
C.Na2FeO4既是氧化产物,又是还原产物
D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com