
【题目】已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol
C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol
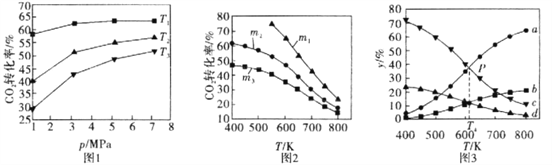
(1)图l、图2分别是CO2的平衡转化率随压强及温度的变化关系,已知m为起始时的投料比,即m=![]() 。
。
①图l中投料比相同,温度从高到低的顺序为________。
②图2中.m1、m2、m3投料比从大到小的顺序为________,理由是________。
(2)图3表示在总压为5MPa的恒压条件下,且m=3时,不同温度下各物质的物质的量分数与温度的关系。
①曲线b代表的物质为________(填化学式)。
②图3中P点时。CO2的转化率为________。
③T4温度时,该反应的平衡常数Kp=________。(提示:用平衡分压代替平衡浓度来计算,某组分平衡分压=总压×该组分的物质的量分数,结果保留小数点后三位)
【答案】 T3>T2>T1 m1>m2>m3 相同温度下,增大氢气的量,平衡正向移动,二氧化碳的转化率增大 CO2 66.7% 0. 243 MPa-4
【解析】本题主要考查化学平衡。
(1)升温,平衡左移,CO2转化率降低,所以①图l中投料比相同,温度从高到低的顺序为T3>T2>T1。
②图2中.m1、m2、m3投料比从大到小的顺序为m1>m2>m3,理由是相同温度下,增大氢气的量,平衡正向移动,二氧化碳的转化率增大。
(2)①升温,平衡左移,CO2、H2增多,CO2增多的程度较小,所以曲线b代表的物质为CO2。
②图3中P点时。H2与H2O的物质的量分数相等,CO2的转化率等于H2的为2/3=66.7%。
③T4温度时,CO2、H2、C2H5OH、H2O的分压p分别是10%5MPa、40%5MPa、10%5MPa、40%5MPa,该反应的平衡常数Kp=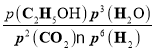 =0.250(MPa)-4。
=0.250(MPa)-4。


科目:高中化学 来源: 题型:
【题目】NA表示阿伏伽德罗常数.下列说法正确的是( )
A.18gNH ![]() 含有质子的数目为10NA
含有质子的数目为10NA
B.1molNa2O2与足量CO2反应时,转移电子的数目为2NA
C.标准状况下,体积均为22.4L的O2、HCl、H2O含有的分子数目均为NA
D.质量为16g的O2和O3的混合气体中所含氧原子的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( ) 
A.WX3和水反应形成的化合物是共价化合物
B.单质的熔点:Y>Z
C.X,Y,R形成的某种化合物可以用于漂白、消毒
D.Y,Z和W三者最高价氧化物对应的水化物能两两相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火箭推进器中装有还原剂肼(N2H4 , 又名联氨)和强氧化剂过氧化氢(H2O2),当它们混合时,立即产生大量氮气和水蒸气,并放出大量热.
(1)写出过氧化氢的电子式;肼的结构式;
(2)已知0.4mol液态肼和足量液态过氧化氢反应,生成氮气和水蒸气时放出256.6KJ的热量,写出反应的热化学方程式;
(3)火箭推进器中的氧化剂还可以用NO2代替.已知有以下反应:①N2(g)+2O2(g)═2NO2(g)△H1=+67.7KJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g)△H2=﹣534KJ/mol
写出肼与NO2反应的热化学方程式;
(4)上述反应应用于火箭推进剂,除释放出大量热量和快速产生大量气体外,还有一个很突出的优点是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉和纤维素都可以用(C6H10O5)n表示,下列叙述正确的是( )
A.它们都不是混合物
B.它们都不是天然高分子化合物
C.它们是同分异构体
D.它们水解的最终产物都是葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用图甲所示装置进行实验,若图乙中横坐标x表示流入电极的电子的物质的量.下列叙述错误的是( ) 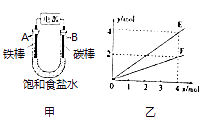
A.E表示反应生成NaOH的物质的量
B.E表示反应消耗H2O的物质的量
C.F表示反应生成H2或Cl2的物质的量
D.F表示反应消耗NaCl的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下: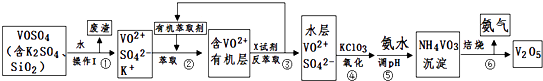
请回答下列问题:
(1)步骤①所得废渣的成分是(写化学式),操作I的名称 .
(2)步骤②、③的变化过程可简化为(下式R表示VO2+ , HA表示有机萃取剂):R2(SO4)n (水层)+2nHA(有机层)2RAn(有机层)+nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是 .
③中X试剂为 .
(3)④的离子方程式为 .
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为 . 若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< . (已知:25℃时,Ksp[Fe(OH)3]=2.6×10﹣39)
(5)该工艺流程中,可以循环利用的物质有和 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体.在同温、同压下,两容器内的气体一定具有相同的是( )
A.原子数
B.相对分子质量
C.质量
D.密度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com