
下列解释事实的离子方程式不正确的是
A.酸性KMnO4溶液与H2O2反应:2MnO4-+5H2O2+6H+= 2Mn2++5O2↑+8H2O
B.向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
C.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
D.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓
D
【解析】
试题分析:A.酸性KMnO4溶液与H2O2反应,根据电荷守恒、电子守恒及原子守恒可得:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,正确;B.向FeBr2溶液中通入足量氯气,阳离子、阴离子都被氧化,反应的离子方程式是:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,正确;C.向FeCl3溶液中加入Mg(OH)2,由于溶解度Fe(OH)3> Mg(OH)2,所以会发生沉淀的转化:3Mg(OH)2+2Fe3+=2Fe(OH)3 +3Mg2+,正确;D.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2,Fe2+、NH4+都会发生反应,离子方程式是:Fe2++2NH4++4OH-=Fe(OH)2↓+2NH3?H2O,错误。
考点:考查离子方程式书写的正误判断的知识。


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源:2014-2015学年上海市虹口区高三上学期期末考试化学试卷(解析版) 题型:选择题
根据右表,以下错误的是
酸 | HF | H3PO4 |
电离常数 | Ki = 3.6×10 - 4 | Ki1= 7.5×10 -3 Ki2= 6.2×10 -8 Ki3= 2.2×10 -13 |
A.NaF和H3PO4反应的产物只有HF、NaH2PO4
B.0.10 mol/L的溶液,pH由大到小的顺序是Na3PO4>Na2HPO4>NaF>NaH2PO4
C.0.10 mol/L的H3PO4溶液中,0.30 mol/L>c(H+)>0.10 mol/L
D.25℃时,等体积、等浓度的NaF和NaH2PO4溶液中所含离子总数前者小于后者
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市长宁区高三上学期教学质量检测化学试卷(解析版) 题型:选择题
某化合物结构简式为 ,下列关于其说法正确的是
,下列关于其说法正确的是
A.分子中碳原子与氮原子的个数比是7∶5
B.属于芳香族化合物
C.能与氢氧化钠溶液反应,但不能与盐酸反应
D.属于苯酚的同系物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省等四校高三第二次联考化学试卷(解析版) 题型:填空题
(8分)已知水在25 ℃和95 ℃时,其电离平衡曲线如图所示。

(1)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为________。
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是________。
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1________α2(填“大于”、“小于”、“等于”或“无法确定”),若二者恰好反应所得溶液的pH<7,原因是__________________。(用离子方程式表示)
(4)在曲线B所对应的温度下,将0.02 mol/L的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省等四校高三第二次联考化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.已知:HI(g)
 H2(g)+
H2(g)+ I2(s) △H =-26.5kJ/mol,由此可知1mol HI气体在密闭容器中充分分解后可以放出26.5kJ的热量
I2(s) △H =-26.5kJ/mol,由此可知1mol HI气体在密闭容器中充分分解后可以放出26.5kJ的热量
B.已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol,则氢气的燃烧热为ΔH=-285.8 kJ/mol
C.肼(N2H4)是一种用于火箭或燃料电池的原料,已知
2H2O(g) + O2(g)=2H2O2(l) △H= +108.3kJ/mol ①
N2H4(l) + O2(g)=N2(g) + 2H2O(g) △H=-534.0kJ/mol ②
则有反应:N2H4(l) + 2 H2O2(l) = N2(g) + 4H2O(l) △H=-642.3kJ/mol
D.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq) = CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省等四校高三第二次联考化学试卷(解析版) 题型:选择题
已知A、B为单质,C为化合物。且有如下转化关系

①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液与Na2CO3溶液反应,放出CO2气体,则A可能是H2
③若C溶液中滴加NaOH溶液,先生成沉淀后又溶解,则B可能为Al
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
能实现上述转化关系的是
A.①② B.②④ C.①③ D.③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东师大附中高三第四次模拟考试理综化学试卷(解析版) 题型:填空题
(16分)用含有A12O3、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。工艺流程如下(部分操作和条件略):
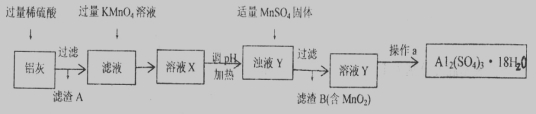
已知:一定条件下,MnO4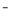 可与Mn2+反应生成MnO2
可与Mn2+反应生成MnO2
(1)稀H2SO4溶解Al2O3的离子方程式是__________________。
(2)已知:生成氢氧化物沉淀的pH如下表(注:金属离子的起始浓度为0.1mol·L-1)

上述流程中,加入过量KMnO4溶液的作用是________________________。(用离子方程式表示)
(3)向滤渣B中加入浓盐酸并加热,能说明沉淀中存在MnO2现象是____________。
上述流程中加入MnSO4体的目的是________________________。
操作a由一系列操作组成,分别是________、________、过滤。
(4)若用沉淀溶解平衡原理分析,操作a能析出A12(SO4)3·18H2O的原因是①____________②___________________
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省曲阜市高三上学期期中考试化学试卷(解析版) 题型:选择题
1.92g铜投人一定盆的浓HNO3中、铜完全溶解,生成的气体颜色越来越浅,共收集到标准状况下672mL气体。将盛有此气休的容器倒扣在水中.通入标准状况下一定体积的氧气恰好使气体完全被水吸收生成硝酸。则通入O2的体积是
A.504mL B.336mL C.224mL D.168mL
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高三12月学情调研化学试卷(解析版) 题型:填空题
(12分)酸浸法制取硫酸铜的流程示意图如下

(1)步骤①中Cu2(OH)2CO3 发生反应的化学方程式为 。
(2)在步骤③发生的反应中,1mol MnO2转移2mol 电子,该反应的离子方程式为 。
(3)该小组为测定黄铵铁矾的组成,进行了如下实验:
a.称取4.800 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
b.量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定
(反应方程式为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
c.量取25.00 mL溶液A,加入足量的NaOH溶液充分反应后,过滤、洗涤、灼烧得红色粉末0.600g。
d.另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥得沉淀1.165 g。
①用Na2S2O3溶液进行滴定时,滴定到终点的颜色变化为 。
②通过计算确定黄铵铁矾的化学式(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com