
| A. | 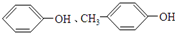 | B. | 甲苯和C3H8O3 | ||
| C. | CH4、C2H4O2 | D. | C3H4、C3H6O |
分析 令烃及烃的含氧衍生物组成通式为CxHyOz,总物质的量一定时,以任意比混合,有机物完全燃烧消耗氧气的物质的量和生成水的物质的量不变,则化学式中的氢原子个数相同,每摩尔有机物耗氧量(x+$\frac{y}{4}$-$\frac{z}{2}$)mol相同即符合题意.
解答 解:A.分子式分别为C6H6O、C7H8O,H原子数不同,故当物质的量之和不变时,生成水的量随着两者的比例的不同而改变,故A错误;
B.1molC7H8燃烧(7+$\frac{8}{4}$)mol=9mol氧气,而1molC3H8O3燃烧消耗(3+$\frac{8}{4}$-$\frac{3}{2}$)mol=$\frac{7}{2}$mol氧气,故当物质的量之和不变时,混合物消耗的氧气的量随着两者的比例的不同而改变,故B错误;
C.1molCH4消耗2mol氧气,1molC2H4O2消耗2mol氧气,且两者中均含4个氢原子,故当两者的物质的量之和不变时,完全燃烧时消耗氧气和生成的水的物质的量也不变,故C正确;
D.C3H4和C3H6O的氢原子数不同,故当两者物质的量之和不变时,生成水的量随着两者的比例的不同而改变,故D错误;
故选C.
点评 本题考查有机物的燃烧计算,为高频考点,侧重考查学生的分析、计算能力的考查,掌握利用燃烧通式法进行的分析解答,本题中学生容易按照总质量一定来解答而出错.


科目:高中化学 来源: 题型:选择题
| A. | dacb | B. | bcad | C. | acbd | D. | dcba |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 铝粉投入到NaOH溶液中:2Al+6H2O+2OH-═2 Al(OH)4-+H2↑ | |
| B. | Al(OH)3溶于NaOH溶液中:Al(OH)3+OH-═Al(OH)4- | |
| C. | NaAl(OH)4溶液中通入足量的CO2:2 Al(OH)4-+CO2═2Al(OH)3↓+CO32-+H2O | |
| D. | Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-═2 Al(OH)4-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3 | B. | NaOH | C. | Na2CO3 | D. | AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
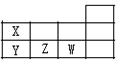
| A. | 原子半径:Y>Z>W | B. | 酸性:HWO4>HXO3>H3YO4 | ||
| C. | 热稳定性:HW>XH3>YH3 | D. | 离子半径:Y3-<Z2-<W- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片、铁片、FeCl3溶液组成的原电池 | |
| B. | 石墨、铁片、FeCl3溶液组成的原电池 | |
| C. | 镁片、锌片、Fe2(SO4)3溶液组成的原电池 | |
| D. | 银片、铁片、Fe(NO3)3溶液组成的原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯塑料的老化是因为发生了加成反应 | |
| B. | 聚乙烯塑料制品可用于食品的包装 | |
| C. | 乙烯和乙烷都能发生加聚反应 | |
| D. | 乙烯分子中所有原子不可能在同一平面内 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
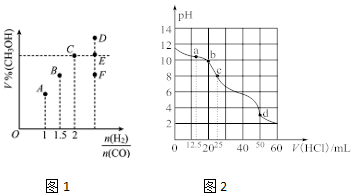
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com