
【题目】下列关于氯气及含氯化合物的说法中,正确的是
A.液氯是氯气的水溶液,它能使干燥的有色布条褪色
B.氯气和NaOH溶液反应可制备消毒液
C.氯气可用于自来水的杀菌消毒,是因为氯气的毒性
D.新制饱和氯水在光照下有气泡产生,其主要成分是氯气
科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的是( )
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C. 蒸发结晶时应将溶液蒸干
D. 称量时,称量物放在称量纸上置于托盘天平的左盘,砝码放在托盘天平的右盘中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组以木炭和浓硝酸为起始原料,探究一氧化氮与过氧化钠反应制备亚硝酸钠。设计装置如下(忽略装置中空气的影响),请回答下列问题:
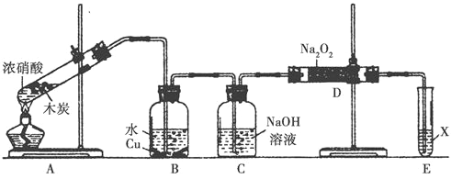
(1)组装好仪器后,必须进行的一项操作是_________________。
(2)装置A的试管中发生反应的化学方程式是_______________。
(3)推测B中可以观察到的主要现象是________;C装置的作用是________。
(4)装置D中除生成NaNO2外,还有另一种固态物质Y,Y的化学式是____________;为了不产生Y物质,可把C装置改为___________(填试剂和仪器名称)。
(5)在酸性溶液中,NO2-可将MnO4-还原为Mn2+。写出有关反应的离子方程式_______________。
(6)E装置中试剂X可以是________。
A.稀硫酸 B.酸性高锰酸钾溶液 C.稀硝酸 D.水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学反应原理的叙述,错误的是( )
A. 使用MnO2作催化剂,可以加快H2O2分解 B. 任何化学反应都有反应热
C. 需要加热才能进行的反应属于吸热反应 D. 铁片的生锈是自发过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年10月10日,中国首届国际山地旅游大会在黔西南州开幕,大会对推动贵州发展生态旅游有着深远的意义。生态旅游的发展需要利用环保的新能源,下列属于新能源的是( )
①天然气 ②太阳能 ③风能 ④石油 ⑤煤 ⑥生物质能 ⑦地热能 ⑧氢能
A.①②③④⑤ B.②③④⑥⑦⑧ C.①②⑤⑥⑦⑧ D.②③⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏伽德罗常数,下列说法正确的是
A.16g氧气和臭氧的混合物中含有的氧原子数为NA
B.标准状况下,22.4 L水中含有的原子数为NA
C.0.5mol/L的H2SO4溶液中含有硫酸分子数目为0.5NA
D.0.1mol氦气所含有的原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)碳、氮和铝的单质及其化合物在工农业生产和生活中有重要用途。
(1)真空碳热还原—氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g) △H=akJ·mol-1
3AlCl(g)═2Al(l)+AlCl3(g) △H=bkJ·mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=_________kJ·mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
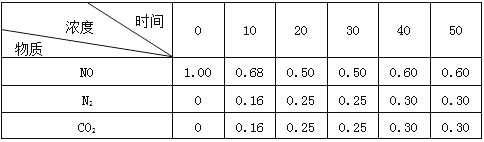
0~10min内,NO的平均反应速率v(NO)= ,T1℃时,该反应的平衡常数K=
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 (填字母编号)。
a.通入一定量的NO
b.通入一定量的N2
c.适当升高反应体系的温度
d.加入合适的催化剂
e.适当缩小容器的体积
③在恒容条件下,能判断该反应一定达到化学平衡状态的依据是 (填选项编号)。
a.单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
b.反应体系的压强不再发生改变
c.混合气体的密度保持不变
d.混合气体的平均相对分子质量保持不变
④若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol/L,则反应达平衡时c(NO)=_________mol/L。NO的转化率_________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.一定条件下某吸热反应能自发进行,说明该反应是熵增大的反应
B.增大反应物浓度可加快反应速率,因此可用浓硫酸与铁反应增大生成H2的速率
C.催化剂可加快反应速率并影响平衡的移动
D.增大反应物固体的量可促使平衡正向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com