


科目:高中化学 来源: 题型:
| A、盛放氢氧化钠溶液的试剂瓶不能用玻璃塞:SiO2+2NaOH═Na2SiO3+H2O | ||||
B、高温下铁与水蒸气反应生成保护膜:2Fe+6H2O(g)
| ||||
| C、工业制取漂粉精:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O | ||||
| D、实验室制取氨气:2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
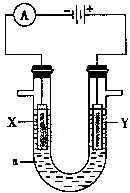 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验要求 | 证明亚硫酸钠氧化变质 | 证明某白色固体中含有NH4+ | 除去铁粉中少量铝粉 | |
| 答案 | Ⅰ | |||
| Ⅱ | . | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀HCl溶液 |
| B、稀Na2SO4溶液 |
| C、CuCl2溶液 |
| D、酸性AgNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com