
分析 酚酞遇碱变红,由NaOH与酸的反应及次氯酸的性质可知,利用继续滴加碱的方法来设计实验,若红色恢复说明酸碱中和使碱减少,若红色不恢复,则说明是次氯酸的作用,以此来解答.
解答 解:用滴管把新制的氯水逐滴加到含有酚酞的氢氧化钠溶液中,当加到最后一滴时,溶液的红色突然消失.若向红色消失的溶液中滴加NaOH溶液后到pH>8.0,恢复红色则说明推测②正确,如溶液仍为无色说明推测①正确,
(1)由上述分析可知,需要NaOH溶液、胶头滴管、pH试纸、玻璃棒,故答案为:B;
(2)进行的实验操作为向已褪色的溶液中滴加NaOH溶液到pH>8.0,故答案为:向已褪色的溶液中滴加NaOH溶液到pH>8.0;
(3)实验现象和结论为滴加NaOH溶液后若溶液恢复红色说明推测②正确,如溶液仍为无色说明推测①正确,故答案为:滴加NaOH溶液后若溶液恢复红色说明推测②正确,如溶液仍为无色说明推测①正确.
点评 本题较简单,考查氯水中酸的性质及次氯酸的漂白性,明确碱遇酚酞变红及氯水的成分、各成分的性质是解答本题的关键.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀. | |
| B. | 向FeCl3溶液中滴加氨水,产生红褐色沉淀;再加入NaHSO4溶液,沉淀消失 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| D. | 分液时,分液漏斗中下层液体从下口流出,上层液体也从下口放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
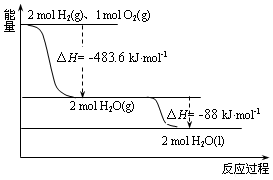
| A. | 氢气的燃烧热△H=-241.8 kJ•mol-1 | |
| B. | 2 mol H2(g)与1 mol O2(g)所具有的总能量比2 mol H2O(g) 所具有的总能量低 | |
| C. | 液态水分解的热化学方程式为:2H2O(l)=2H2(g)+O2(g)△H=+571.6 kJ•mol-1 | |
| D. | H2O(g)生成H2O(l)时,断键吸收的能量小于成键放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸显弱酸性,可用于雕刻玻璃 | |
| B. | NaClO溶液显碱性,可用于杀菌消毒 | |
| C. | NH4Cl分解时吸收大量的热,可用作阻燃剂 | |
| D. | CO2密度比空气大,可用作镁着火时的灭火剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
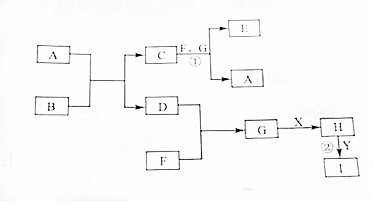 有关物质的转化关系如图所示(部分物质与条件已略去).其中A,D,F,G为常见的气体,D为单质,A,F,G为氧化物,G为棕红色;B为淡黄色固体.X是最常见的液体,Y是常见的金属单质,I溶液为蓝色,
有关物质的转化关系如图所示(部分物质与条件已略去).其中A,D,F,G为常见的气体,D为单质,A,F,G为氧化物,G为棕红色;B为淡黄色固体.X是最常见的液体,Y是常见的金属单质,I溶液为蓝色, .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com