
| A. | 7.8克Na2O2加入100克水中所得溶液中含氧原子0.2NA个 | |
| B. | 标准状况下,11.2LCCl4中含2NA个σ键 | |
| C. | 用惰性电极电解氯化铜溶液,当阳极产生标准状况下黄绿色气体6.72L时,则电路中转移的电子数为0.6NA | |
| D. | 将20.00mL1.5mol/LFeCl3溶液制成胶体,则所得胶体中含有0.03NA个胶粒 |
分析 A.溶液中水分子也含氧原子;
B.标准状况下四氯化碳不是气体;
C.电解硫酸铜溶液时,阳极生成的为氯气,标况下6.72L氯气的物质的量=$\frac{6.72L}{22.4L/mol}$=0.3mol,生成0.3mol氯气需要电子转移0.6mol电子;
D.20.00mL1.5mol/LFeCl3溶液中氯化铁物质的量=0.0200L×1.5mol/L=0.03mol,水解生成的氢氧化铁胶体分散质为氢氧化铁的集合体.
解答 解:A.7.8克Na2O2加入100克水中所得溶液中,过氧化钠和水反应生成氢氧化钠和氧气,得到溶液中水分子含氧原子,则含氧原子数大于0.2NA个,故A错误;
B.标准状况下,四氯化碳不是气体,11.2LCCl4中物质的量不是0.5mol,故B错误;
C.电解硫酸铜溶液时,阳极生成的为氯气,标况下6.72L氯气的物质的量=$\frac{6.72L}{22.4L/mol}$=0.3mol,阳极的电极反应为2Cl--2e-=Cl2↑,则电路中转移的电子数为0.6NA,故C正确;
D.氢氧化铁胶体分散质为氢氧化铁的集合体,20.00mL1.5mol/LFeCl3溶液中氯化铁物质的量=0.0200L×1.5mol/L=0.03mol,所得胶体小于0.03NA个,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系.


科目:高中化学 来源: 题型:选择题
| A. | 一定条件下乙醇和氧气反应生成乙醛 | |
| B. | 乙烯通入溴水中 | |
| C. | 乙烯合成聚乙烯 | |
| D. | 光照射甲烷和氯气的混合气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用蒸馏的方法除去乙酸中少量的乙醇 | |
| B. | 可选用KOH溶液除去氧化铁中混杂的氧化铝 | |
| C. | 可用过滤的方法除去粗盐溶液中的泥沙 | |
| D. | 可用萃取、分液、蒸馏的方法从稀碘水获得单质碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 惰性电极电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2+═4Na++2Cu(OH)2↓+O2↑ | |
| C. | 向NaClO和NaCl混合溶液中滴少量FeSO4溶液:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| D. | 向KAl(SO4)2溶液中滴加Ba(OH)2溶液至沉淀物质的量最大:Al3++2SO42-+2Ba2++4OH-═[Al(OH)4]-+2BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 装置 | 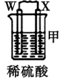 |  | 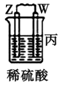 |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
| A. | 装置甲中X电极附近有气泡产生 | |
| B. | 装置乙中Y电极上的反应式为Cu2++2e-=Cu | |
| C. | 装置丙中溶液的pH增大 | |
| D. | 四种金属的活动性强弱顺序为W>X>Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④ | C. | ①③ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ①②④ | C. | ②③⑤⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3固体 | B. | Zn粉 | C. | K2SO4固体 | D. | CuSO4晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com