
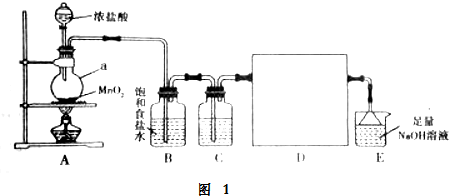
分析 制备干燥纯净的氯气并验证氯气的性质,装置图分析可知,A氯气制备氯气的装置,制备得到氯气中含氯化氢、水蒸气,通过装置B中的饱和食盐水除去氯化氢气体,通过装置C中的浓硫酸吸收水蒸气,最后剩余氯气用氢氧化钠溶液吸收,
(1)图1中仪器a的形状和用途分析为圆底烧瓶;
(2)装置B是除去氯化氢气体,装置C是吸收水蒸气;
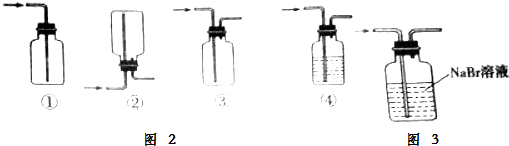
(3)氯气溶于水,密度比空气大,可以用向上排气法收集,也可以用排饱和食盐水的方法收集;
(4)氯气通入溴化钠溶液发生氧化还原反应生成溴单质,溶液变化为橙红色,在溶液中加入苯或四氯化碳有机溶剂萃取分液分离溴单质,有机萃取分液操作选择玻璃仪器;
(5)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,检验溶液中氯离子的存在需要排除氢氧化钠、次氯酸根离子的干扰;
解答 解:制备干燥纯净的氯气并验证氯气的性质,装置图分析可知,A氯气制备氯气的装置,制备得到氯气中含氯化氢、水蒸气,通过装置B中的饱和食盐水除去氯化氢气体,通过装置C中的浓硫酸吸收水蒸气,最后剩余氯气用氢氧化钠溶液吸收,
(1)图1中仪器名称为圆底烧瓶,
故答案为:圆底烧瓶;
(2)氯气在饱和食盐水中溶解度减小,装置B中饱和食盐水是用来除去氯化氢气体,装置C中的浓硫酸是吸收水蒸气用来得到干燥的氯气,
故答案为:除去氯气中的氯化氢气体;浓硫酸;
(3)氯气溶于水,密度比空气大,可以用向上排气法收集,也可以用排饱和食盐水的方法收集,装置中①无气体排出口,不能用来收集气体,装置②是向下排空气法收集气体,不符合氯气收集,装置③导气管长进短出,可以收集比空气重的气体,装置④导气管长进短出不能收集到气体,故答案为:③;
(4)氯气通入溴化钠溶液发生氧化还原反应生成溴单质,Cl2+2NaBr=Br2+2NaCl,溶液变化为橙红色,在溶液中加入苯或四氯化碳有机溶剂萃取分液分离溴单质,有机萃取分液操作选择玻璃仪器为分液漏斗、烧杯,
故答案为:溶液变橙红色;萃取分液;分液漏斗、烧杯;
(5)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,检验溶液中氯离子的存在需要排除氢氧化钠、次氯酸根离子的干扰,取少量溶液少许于试管中,加入硝酸镁沉淀完全后静置后,在上层清液中滴入硝酸银溶液,若上层白色沉淀证明溶液中含氯离子,
故答案为:取少量烧杯溶液中溶液于试管中,加入硝酸镁溶液静置后在上层清液中加入硝酸银溶液若上层白色沉淀证明含氯离子;
点评 本题考查了实验室氯气的制备、气体除杂、气体干燥、气体收集、离子检验等知识,掌握基础是解题关键,题目难度中等.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | v(HI)=0.8 mol•Lˉ1•sˉ1 | B. | v(I2)=0.2 mol•Lˉ1•sˉ1 | ||
| C. | v(HI)=0.1 mol•Lˉ1•minˉ1 | D. | v(H2)=0.05 mol•Lˉ1•sˉ1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含质子数Z+A | B. | 所含电子数Z+n | C. | 所含中子数 A-Z | D. | 质量数Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
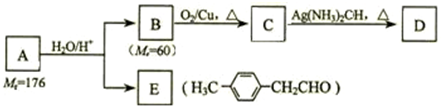
 .
. 、
、 、
、 (其中一种).
(其中一种).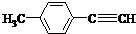 )的一条路线如下:
)的一条路线如下: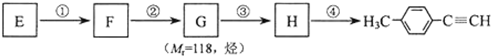
 ;
;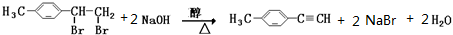 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 原子团 | -CH2- | 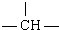 |  | -CH3 | -NH2 | -COOH |
| 个数 | n | m | p | a | 1 | 1 |
| A. | m+2p | B. | n+m+p | C. | n+m+2p | D. | 2n+3m+4p |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
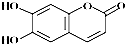
| A. | M的分子式为C9H8O4 | |
| B. | 1 mol M最多能与2 molBr2发生反应 | |
| C. | M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 | |
| D. | 1 mol M与足量NaHCO3反应能生成2 mol CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体中105B和115B两种同位素原子的质量比为1:4 | |
| B. | 5.4 g该晶体硼所含中子为2.9 mol | |
| C. | 等质量的分别由105B和115B构成的晶体硼所含中子数之比为5:6 | |
| D. | 若碳原子质量为w g,则105B原子的质量为 $\frac{10w}{12}$g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com