
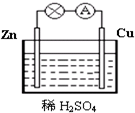
 图为原电池的示意图.请回答:
图为原电池的示意图.请回答:分析 (1)锌铜原电池依据装置图分析,锌做负极失电子发生氧化反应生成锌离子;
(2)铜做正极,溶液中氢离子得到电子生成氢气,发生还原反应,电子流向从负极沿导线流向正极,溶液中阳离子移向正极;
(3)原电池工作时,因正极发生2H++2e-=H2↑;
(4)如Zn棒质量减轻3.25g,n(Zn)=$\frac{3.25g}{65g/mol}$=0.05mol,由Zn-2e-=Zn2+可知,转移2mol电子,则由2H++2e-=H2↑可知,生成1mol氢气,体积为22.4 L.
解答 解:(1)锌铜原电池依据装置图分析,锌做负极失电子发生氧化反应生成锌离子,负极发生的反应是Zn-2e-=Zn2+,
故答案为:负;Zn-2e-=Zn2+;氧化反应;
(2)铜做正极,溶液中氢离子得到电子生成氢气,发生还原反应,电子流向从负极沿导线流向正极,溶液中阳离子移向正极;
故答案为:电子;铜片;
(3)原电池工作时,因正极发生2H++2e-=H2↑,则硫酸浓度减小,故答案为:减小;
(4)如Zn棒质量减轻3.25g,n(Zn)=$\frac{3.25g}{65g/mol}$=0.05mol,由Zn-2e-=Zn2+可知,转移2mol电子,则由2H++2e-=H2↑可知,生成1mol氢气,体积为22.4 L,所以转移电子的物质的量为0.05×2=0.1mol,生成气体体积为:1.12L;
故答案为:1.12L.
点评 本题考查了原电池原理的分析应用主要是电极反应,电极判断,电子流向,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:填空题
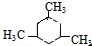 .
.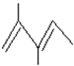 .
.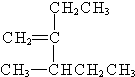 3-甲基-2-乙基-1-戊烯;
3-甲基-2-乙基-1-戊烯; 2,2,6-三甲基-4-乙基辛烷.
2,2,6-三甲基-4-乙基辛烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X为0.25 mol•L-1 | |
| B. | Y为0.1 mol•L-1 | |
| C. | Z为0.2 mol•L-1 | |
| D. | Z为0.25 mol•L-1时,Y为0.45 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同质量的乙炔和苯完全燃烧生成二氧化碳的质量完全相等 | |
| B. | 都容易发生取代反应 | |
| C. | 苯只能在特殊条件下发生加成反应 | |
| D. | 苯不能被KmnO4所氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
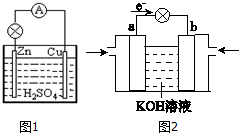 原电池是直接把化学能转化为电能的装置.
原电池是直接把化学能转化为电能的装置.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、
、
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠的还原性很强,可以用来冶炼金属钛、锆、铌等 | |
| B. | 钠的化学性质非常活泼,钠元素只能以化合态存在于自然界 | |
| C. | 钠极易和水反应而被还原 | |
| D. | 钠、氧化钠、氢氧化钠的焰色反应均显黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子晶体中一定存在范德华力和共价键两种作用力,可能存在氢键 | |
| B. | 某晶体熔融态能导电,则一定是离子晶体 | |
| C. | 分子晶体、原子晶体、离子晶体、金属晶体都可以采用紧密堆积方式 | |
| D. | 金属元素形成的化合物可能是分子晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com