
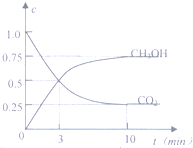
 Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1L�Ŀͱ������У�����1molCO2��3molH2����500���·�����Ӧ��CO2��g��+3H2O��g��?CH3OH��g��+H2O��g����
Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1L�Ŀͱ������У�����1molCO2��3molH2����500���·�����Ӧ��CO2��g��+3H2O��g��?CH3OH��g��+H2O��g����| ��c |
| ��t |
| 2.25mol |
| 10min |
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 |
| ���ܼ����� |  |  |  |  |  |  |
| ÿ����Ƥ���϶����������� | ||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
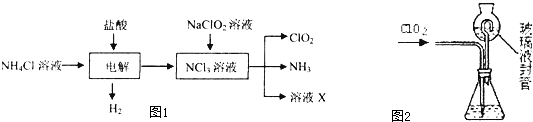
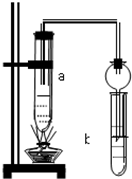 ��ͼ��ʾ�����Թ�a���ȼ�2mL�Ҵ�����ҡ����������5mLŨ���ᣬҡ����ȴ���ټ���2g��ˮ�����ƣ���ֽ����̶�������̨�ϣ����Թ�b�м��������ı���Na2CO3��Һ�����Ӻ�װ�ã���a���ȣ����۲쵽�Թ�b������������ʱ��ֹͣʵ�飮
��ͼ��ʾ�����Թ�a���ȼ�2mL�Ҵ�����ҡ����������5mLŨ���ᣬҡ����ȴ���ټ���2g��ˮ�����ƣ���ֽ����̶�������̨�ϣ����Թ�b�м��������ı���Na2CO3��Һ�����Ӻ�װ�ã���a���ȣ����۲쵽�Թ�b������������ʱ��ֹͣʵ�飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n��HI��/mol | 0.180 | 0.164 | 0.152 | 0.144 | 0.140 | 0.140 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
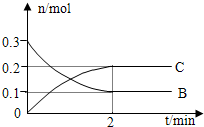 һ���¶��£���2L���ܱ������з�����Ӧ��A��g��+2B��g��?xC��g����H��0��B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ�������й�˵������ȷ���ǣ�������
һ���¶��£���2L���ܱ������з�����Ӧ��A��g��+2B��g��?xC��g����H��0��B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ�������й�˵������ȷ���ǣ�������| A��x=2 |
| B��2min�����¶�ƽ�������ƶ� |
| C����Ӧ��ʼ2min�ڦͣ�C��=0.1mol/��L?min�� |
| D���������ڻ������ѹǿ���ٸı�ʱ����Ӧ��ϵ�ﵽ��ѧƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ֻ�Т�?? |
| B��ֻ�Т٢�?? |
| C��ֻ�Т٢ڢ�?? |
| D��ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NH4++H2O?NH3?H2O+H+ |
| B��HCO3-+H2O?CO32-+H3O+ |
| C��S2-+H2O?HS-+OH- |
| D��NH3+H2O?NH4++OH- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com