
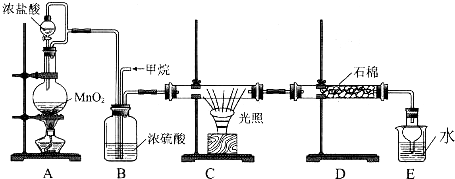
分析 甲烷与氯气在光照的条件下发生取代反应生成多种氯代甲烷和氯化氢.A装置是浓盐酸和二氧化锰制取氯气的发生装置,通过B装置,除去氯气中的水蒸气,控制两种气体的流速,使氯气和甲烷混合均匀,C装置是甲烷和氯气发生取代反应的装置,D装置盛有湿润的KI粉末可以用来除去过量的氯气,尾气中含有有毒气体CH3Cl和过量的甲烷,容易污染空气,需要进行尾气处理.
(1)MnO2能将HCl(浓)氧化为MnCl2和Cl2;
(2)甲烷可以和氯气放生取代反应生成一氯甲烷、二氯甲烷、三氯甲烷、三氯甲烷和氯化氢;
(3)氯气具有强氧化性,能将碘离子氧化生成碘单质,所以D装置的石棉中均匀混有KI粉末,其作用是吸收过量的氯气;
(4)尾气中含有有毒气体CH3Cl和过量的甲烷,容易污染空气,需要进行尾气处理;
(5)盐酸和有机物不能互溶,所以可以采用分液的方法分离;
(6)根据四种取代物的物质的量相等结合碳原子守恒计算取代物的物质的量,再根据被取代的氢原子和氯气分子之间的关系式计算消耗氯气的物质的量;
解答 解:甲烷与氯气在光照的条件下发生取代反应生成多种氯代甲烷和氯化氢.A装置是浓盐酸和二氧化锰制取氯气的发生装置,通过B装置,除去氯气中的水蒸气,控制两种气体的流速,使氯气和甲烷混合均匀,C装置是甲烷和氯气发生取代反应的装置,D装置盛有湿润的KI粉末可以用来除去过量的氯气,尾气中含有有毒气体CH3Cl和过量的甲烷,容易污染空气,需要进行尾气处理.
(1)MnO2能将HCl(浓)氧化为MnCl2和Cl2,A中制取Cl2反应的化学方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)甲烷与氯气反应生成一氯甲烷的方程式为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl,
故答案为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl;
(3)湿润的KI粉末可以用来除去过量的氯气,发生反应:2KI+Cl2=2KCl+I2,
故答案为:除去过量的氯气;
(4)由于上述过程中产生的氯气和HCl均易导致大气污染,所以E的作用是吸收尾气,HCl极易溶于水易发生倒吸,所以E还可以防止倒吸,
故答案为:C;
(5)E装置中除了有盐酸生成外,还含有二氯甲烷、三氯甲烷和四氯化碳,二氯甲烷、三氯甲烷和四氯化碳不溶于水,能分层,可用分液分开,
故答案为:分液;
(6)1mol甲烷完全与氯气发生取代反应,若生成相同物质的量的四种取代物,所以每种取代物的物质的量是0.25mol,甲烷和氯气的取代反应中,被取代的氢原子的物质的量与氯气的物质的量相等,所以生成0.25mol一氯甲烷需要氯气0.25mol氯气,生成0.25mol二氯甲烷需要氯气0.5mol,生成0.25mol三氯甲烷需要氯气0.75mol氯气,生成0.25mol四氯化碳需要氯气1mol,所以总共消耗氯气的物质的量=0.25mol+0.5mol+0.75mol+1mol=2.5mol,
故答案为:2.5mol;
点评 本题考查氯气的制备以及甲烷与氯气的取代反应,题目难度中等,本题注意实验的原理,以及甲烷的取代反应中被取代的氢原子和氯气之间的关系.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:解答题
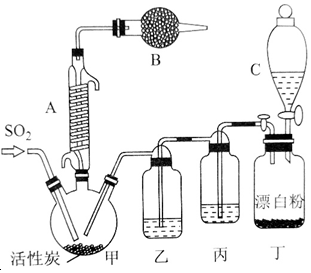 有关信息如下:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解.回答下列问题:
有关信息如下:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 在稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ | |
| C. | 由C(s,石墨)=C(s,金刚石)△H=+1.90kJ/mol可知,石墨没有金刚石稳定 | |
| D. | 在101kPa时,2g的氢气完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①②③ | C. | ②④ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4是还原剂 | B. | CO是氧化剂 | ||
| C. | 1mol Fe3O4得到6mol电子 | D. | 4molCO失去8mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以用四氯化碳把溴水中的溴萃取出来,振荡静置分层后,下层液体为无色 | |
| B. | 萃取分液时,从分液漏斗下口流完下层液体,及时关闭.再打开流出上层液体 | |
| C. | 碘易溶于酒精,微溶于水,故可以用酒精萃取碘水中的碘 | |
| D. | 萃取之后,一般通过分液漏斗将互不相溶的液体分离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com